酸碱盐复习材料,2份复习课件,30套单元测试卷,拿走不谢!转给有需要的人!
- 2026-04-30 10:28:04












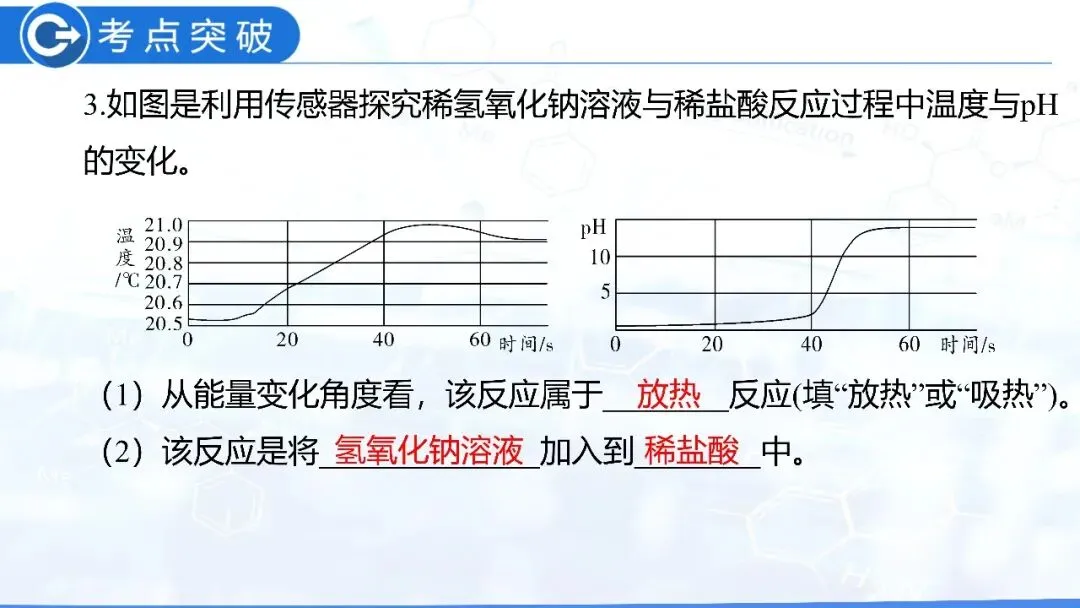

盐酸 | 硫酸 | |
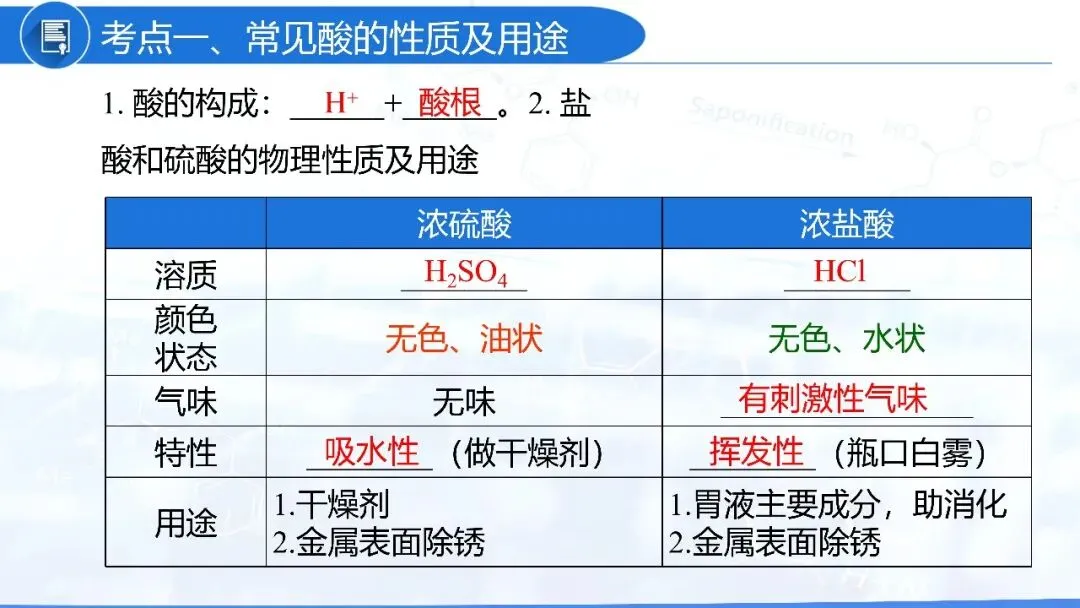
化学式 | HCl | H2SO4 |
形成 | H2+Cl2HCl | SO2+H2O=H2SO3,2H2SO3+O2=2H2SO4 (酸雨形成的原理) |
状态 | 无色液体、具有酸味、刺激性气味 | (浓硫酸)无色粘稠的油状液体 (稀硫酸)无色液体 |
特点 | 浓盐酸具有强挥发性 | 浓硫酸具有吸水性(物理性质) 浓硫酸具有强腐蚀性(化学性质) 浓硫酸溶于水时会放出大量热 |
用途 | 重要化工产品,用于金属表面除锈、制药 人体胃液中含有盐酸,可以帮助消化 | 重要化工原料,用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等 在实验室中常用浓硫酸作干燥剂 |
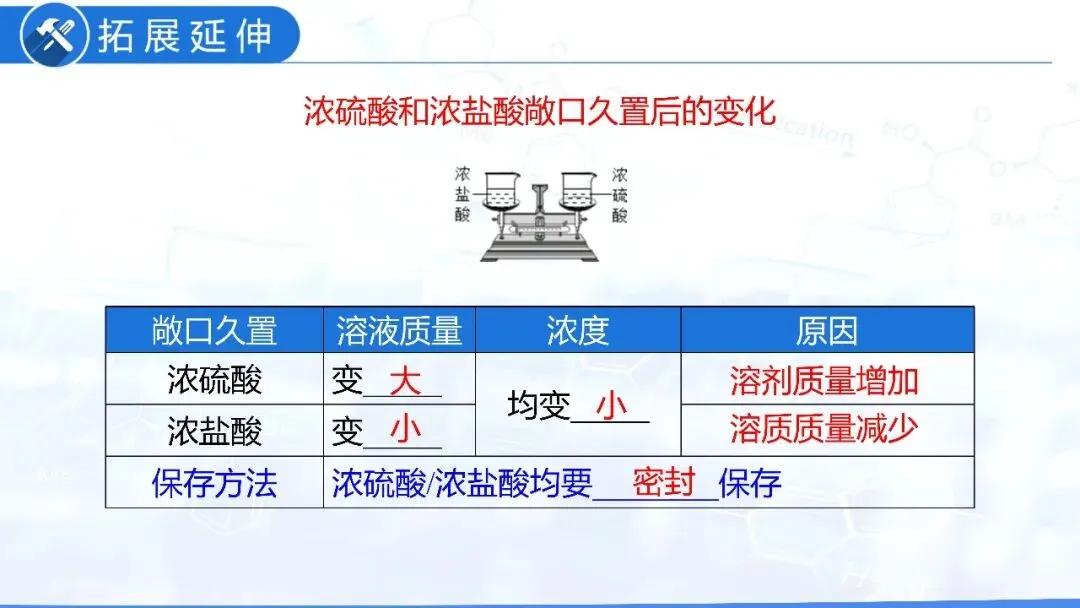
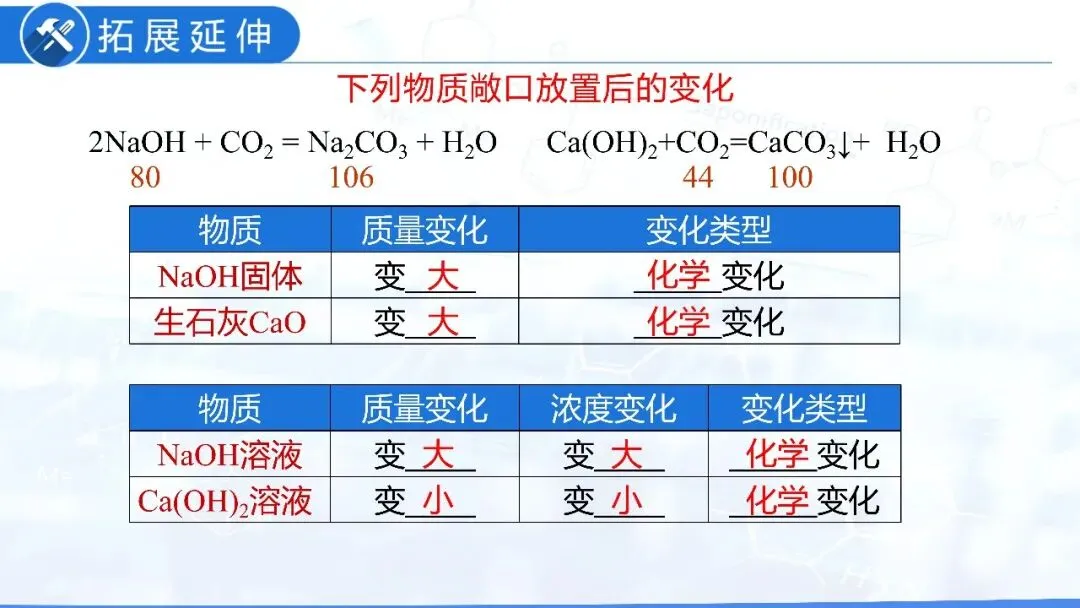
敞口放置的变化 | 质量减小,溶质质量分数减小(挥发性) | 质量变大,溶质质量分数减小(吸水性) |
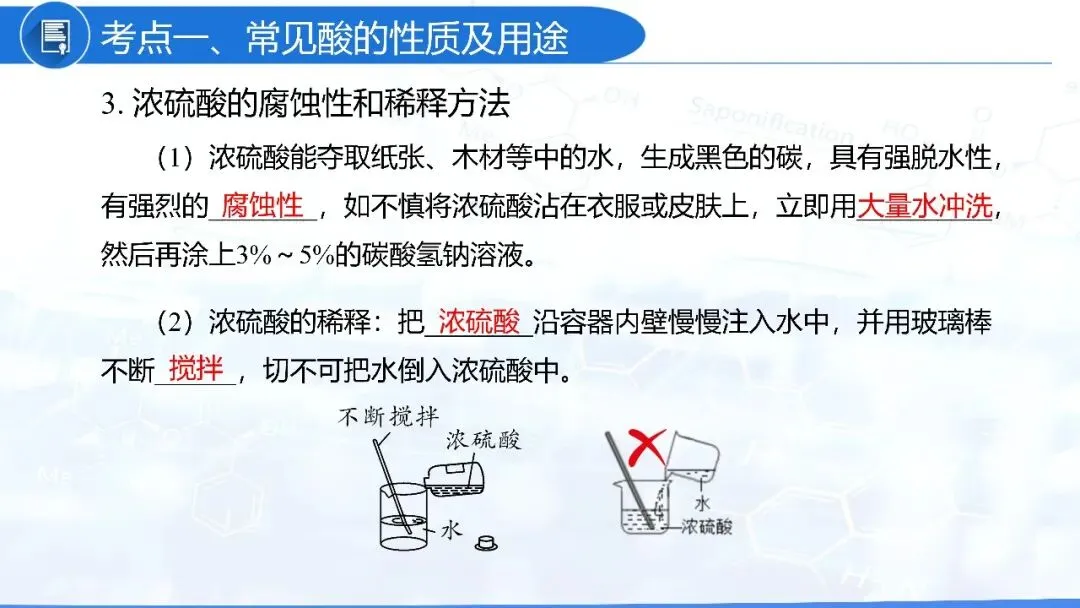
注意事项 | 工业生产的盐酸偏黄,是因为含有Fe3 +,可用蒸馏法提纯。 打开浓盐酸的瓶塞,会有白雾出现,是因为:挥发的氯化氢气体极易溶于水,挥发时溶解的氯化氢与水蒸气形成了盐酸的小液滴。 | 浓硫酸的稀释:把浓硫酸沿器壁慢慢注入,并不断用玻璃棒搅拌(目的:加快溶解、散热)。 如果把水倒进浓硫酸里,由于水的密度小,浮在硫酸上面,硫酸溶解时放出的热不易散失,使水暴沸,使硫酸液滴向四周飞溅,导致危险。 |
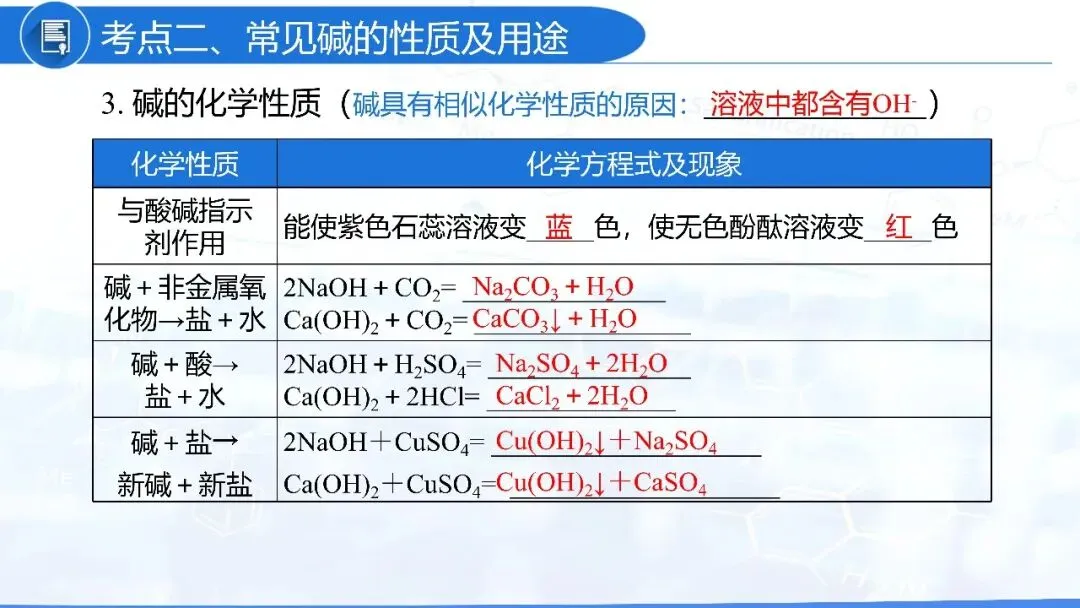
氢氧化钠(烧碱、火碱、苛性钠) | 氢氧化钙(消石灰、熟石灰) | |
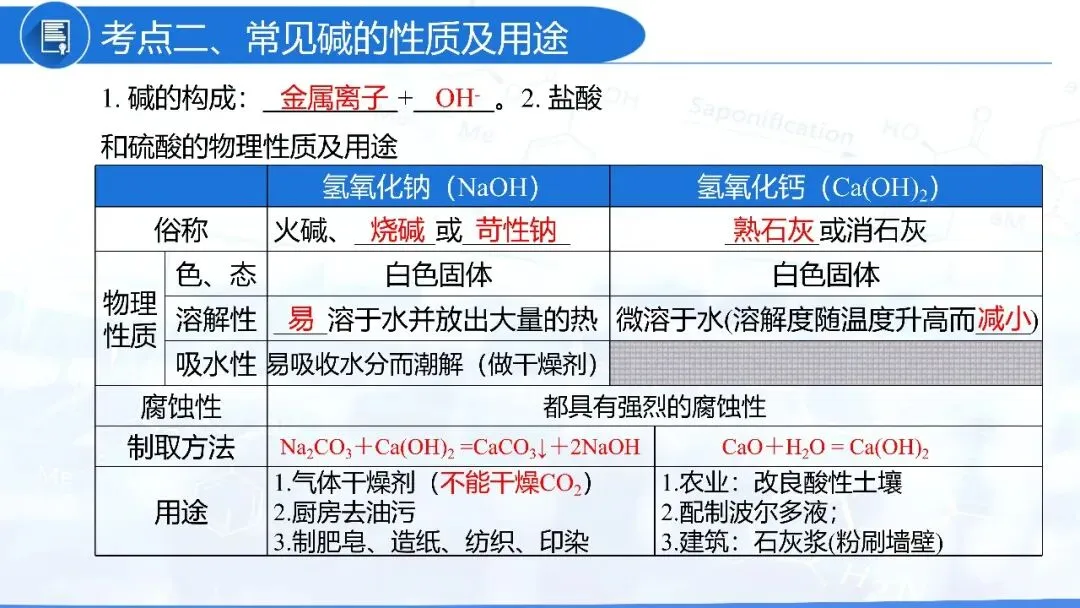
化学式 | NaOH | Ca(OH)2 |
工业制法 | Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ | CaCO3CaO+CO2↑,CaO+H2O=Ca(OH)2 |
状态 | 白色块状固体 | 白色粉末状固体 |
腐蚀性 | 强腐蚀性 | 较强腐蚀性 |
特点 | 极易溶于水,溶于水时放出大量的热。 氢氧化钠固体易吸水而潮解。 | 微溶于水,溶于水时放热不明显。 |
用途 | 用于肥皂、石油、造纸、纺织和印染等行业(除玻璃方面外,用途与纯碱类似)。 氢氧化钠能与油脂反应,所以可以除油污。 | 漂白粉、建筑材料、改良酸性土壤和河流、配制波尔多液 在实验室中可以证明二氧化碳。 |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | |
厕所清洁剂 | 柠檬 醋 | 苹果 | 橘子 | 酱油 | 西瓜 | 牛奶 | 鸡蛋清 | 牙膏 | 肥皂 | 草木灰水 | 厨房清 洁剂 |
实验操作 | 现象 | 结论 |
①取烘干后的固体于烧杯中,加足量的水,搅拌、静置 | 不放热 | 烘干后的固体中不存在___。 |
②取静置后的上层清液。滴入_______。 | 清液____。 | 烘干后的固体中存在Ca(OH)2 |
③取静置后的底部固体。加足量_______。 | 有气泡产生 | 烘干后的固体中存在_____。 |







: https://pan.baidu.com/s/1xaLM4yn8hBdvObJpw0I3KA 提取码: czhx
--来自百度网盘超级会员v1的分享







