新标准《检验检测机构内部审核》课件PPT
- 2026-04-10 04:30:58
2.12.1检验检测机构应当依据法律法规、标准(包括但不限于国家标准、行业标准、国际标准)的规定制定完善的管理体系文件,包括政策、制度、计划、程序和作业指导书等。检验检测机构建立的管理体系应当符合自身实际情况并有效运行。
2.12.1-28)检验检测机构建立的管理体系应当有效运行,具有体系运行相应的记录。
...
f) 检验检测机构管理体系内部审核记录;
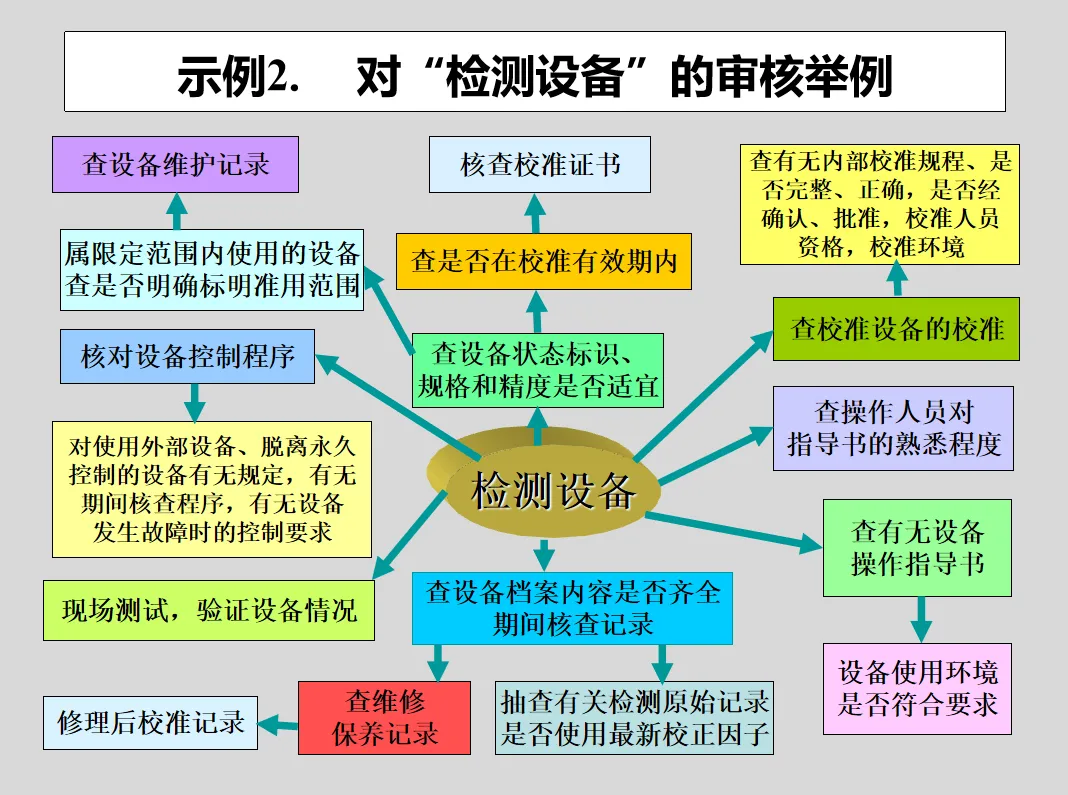
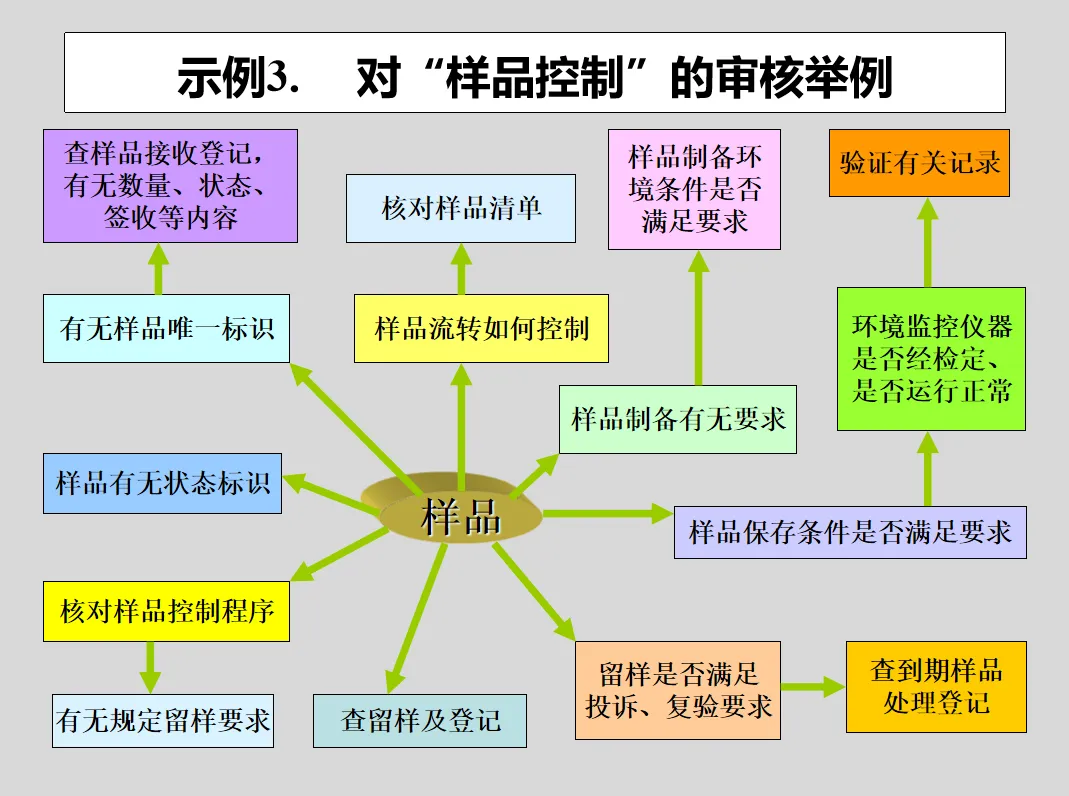
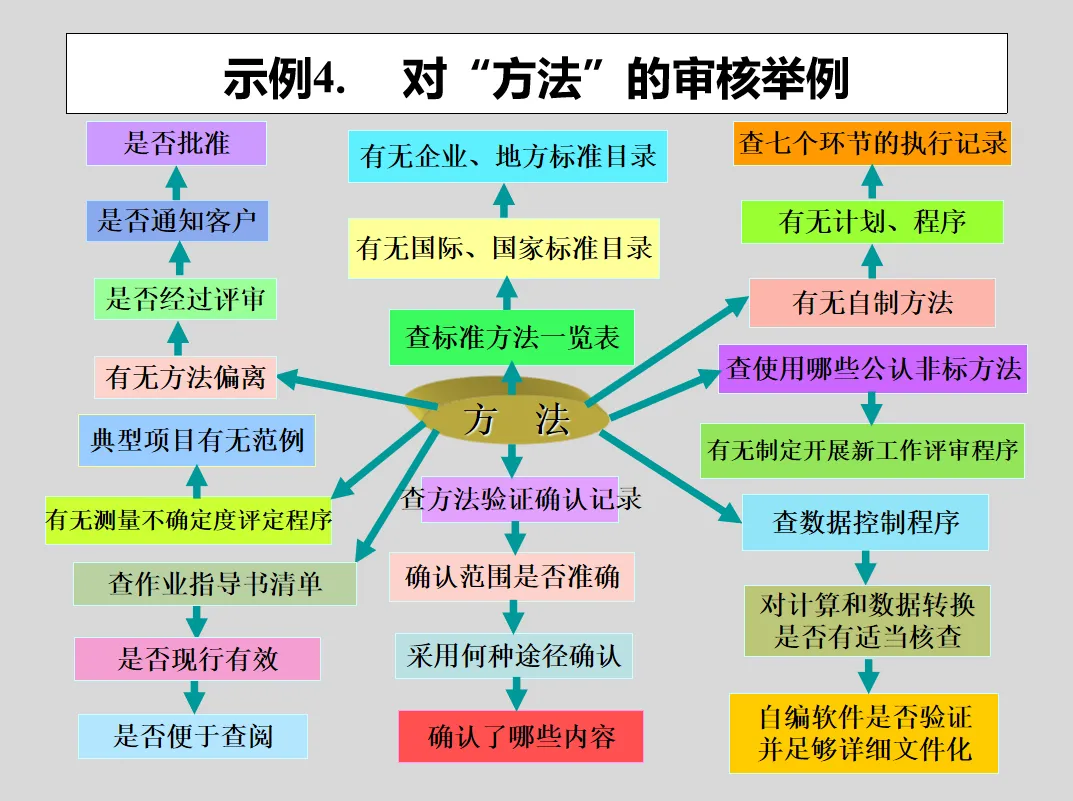
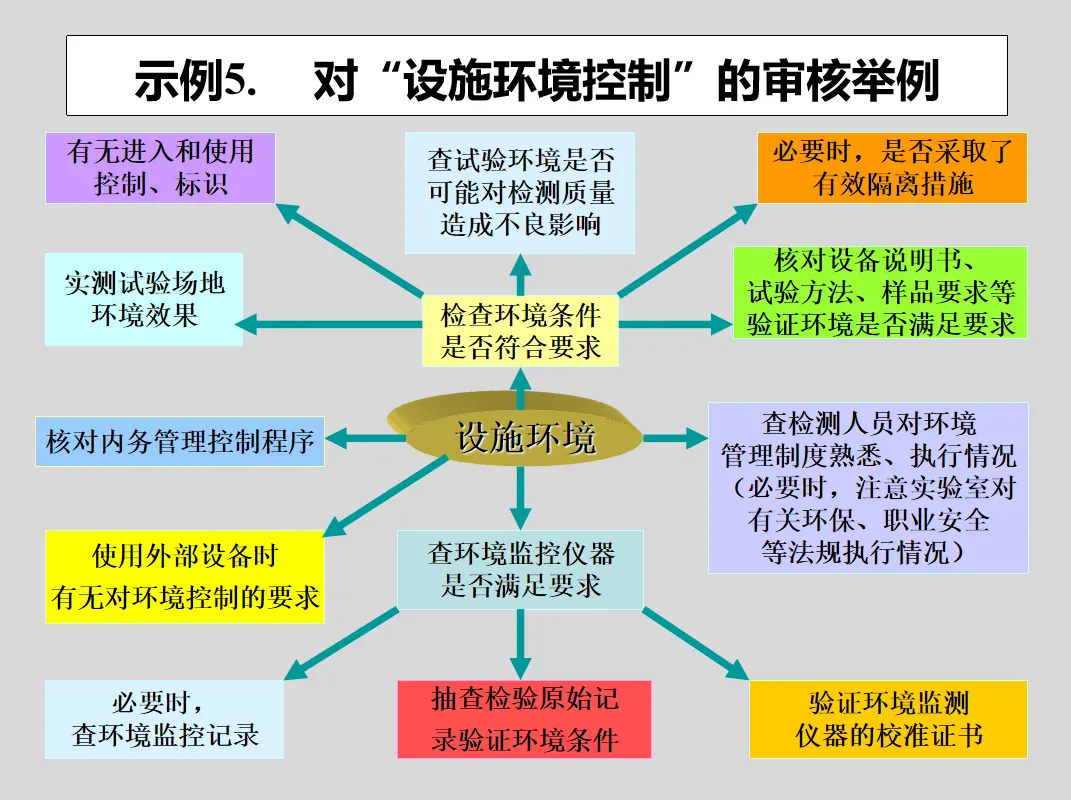
GB/T 27025-2019《检测和校准实验室能力的通用要求》(ISO17025:2017、CNAS-CL01:2018)对内审的要求:
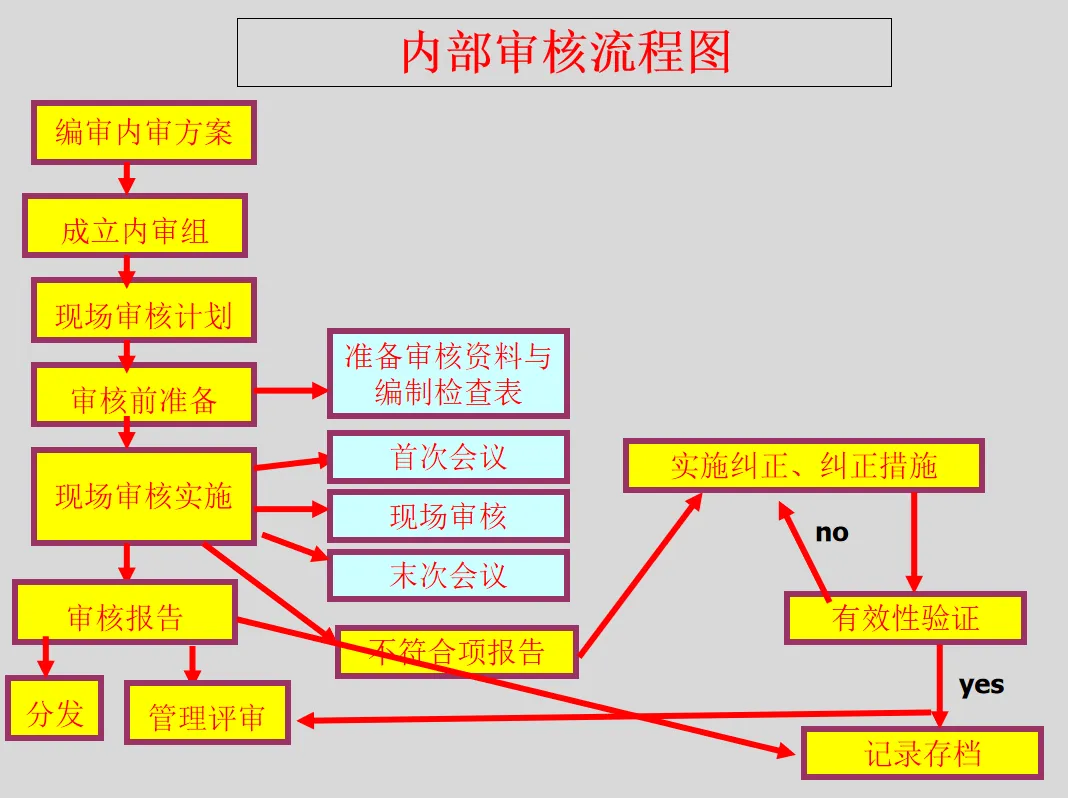
8.8 内部审核(方式 A)
8.8.1 实验室应按照策划的时间间隔进行内部审核,以提供有关管理体系的下列信息:
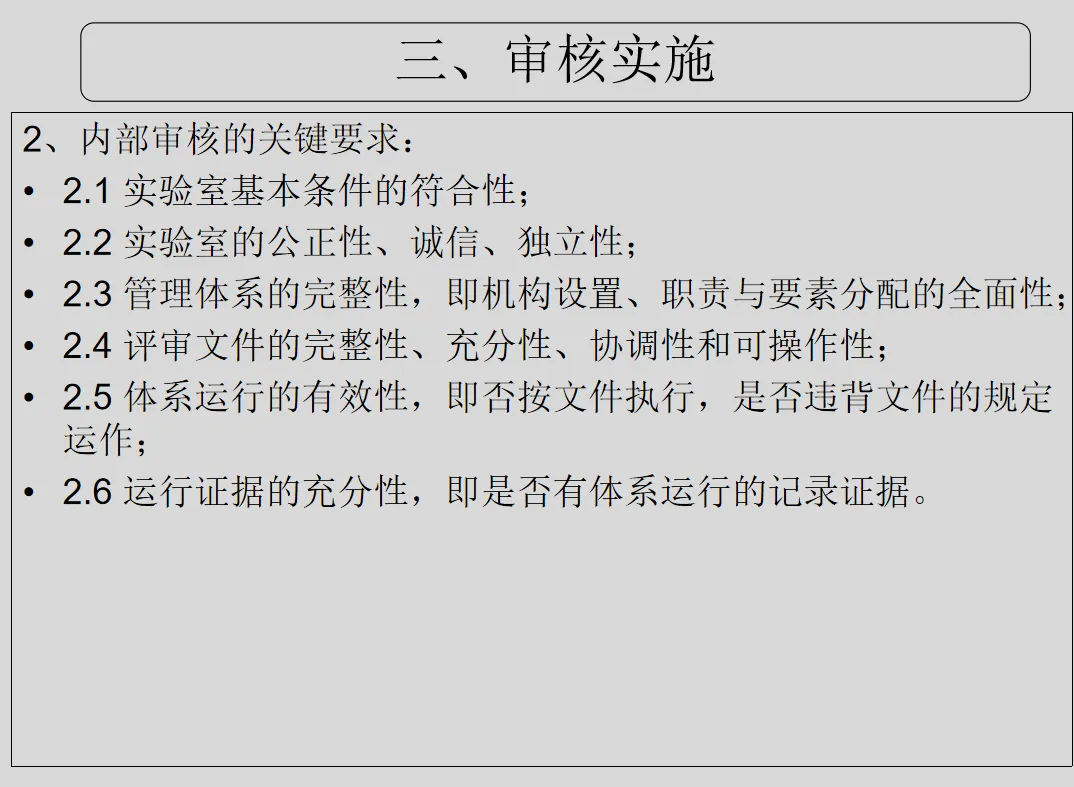
a) 是否符合:
——实验室自身的管理体系要求,包括实验室活动;
——本准则的要求; ---符合什么(2个方面)
b) 是否得到有效的实施和保持。 ---实施和保持
8.8.2 实验室应:
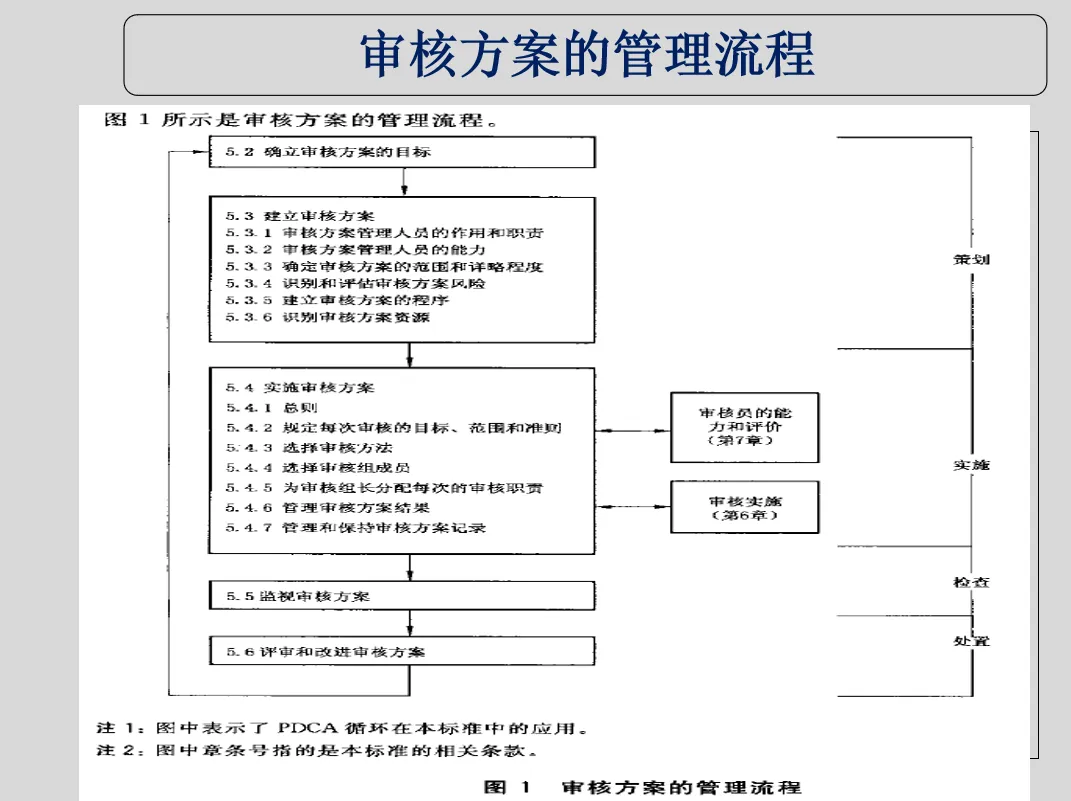
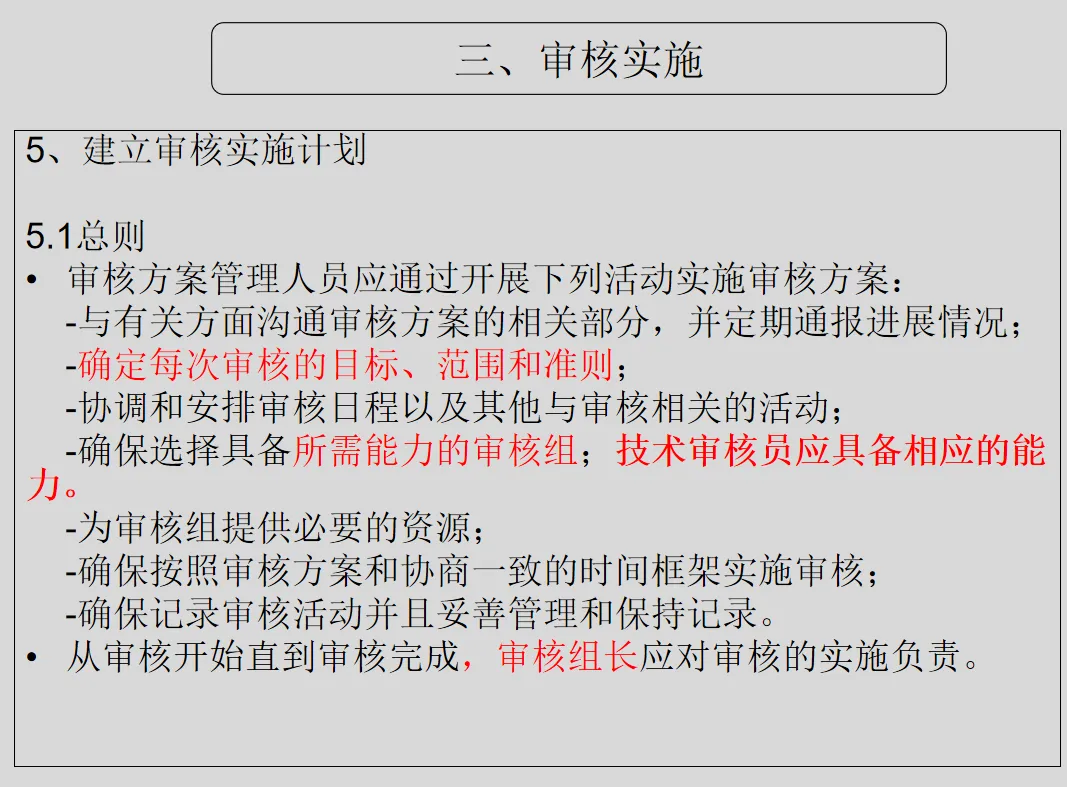
a) 考虑实验室活动的重要性、影响实验室的变化和以前审核的结果,策划、制定、实施和保持审核方案,审核方案包括频次、方法、职责、策划要求和报告;
b) 规定每次审核的审核准则和范围(时间、部门、要素等);
c) 确保将审核结果报告给相关管理层;
d) 及时采取适当的纠正和纠正措施;
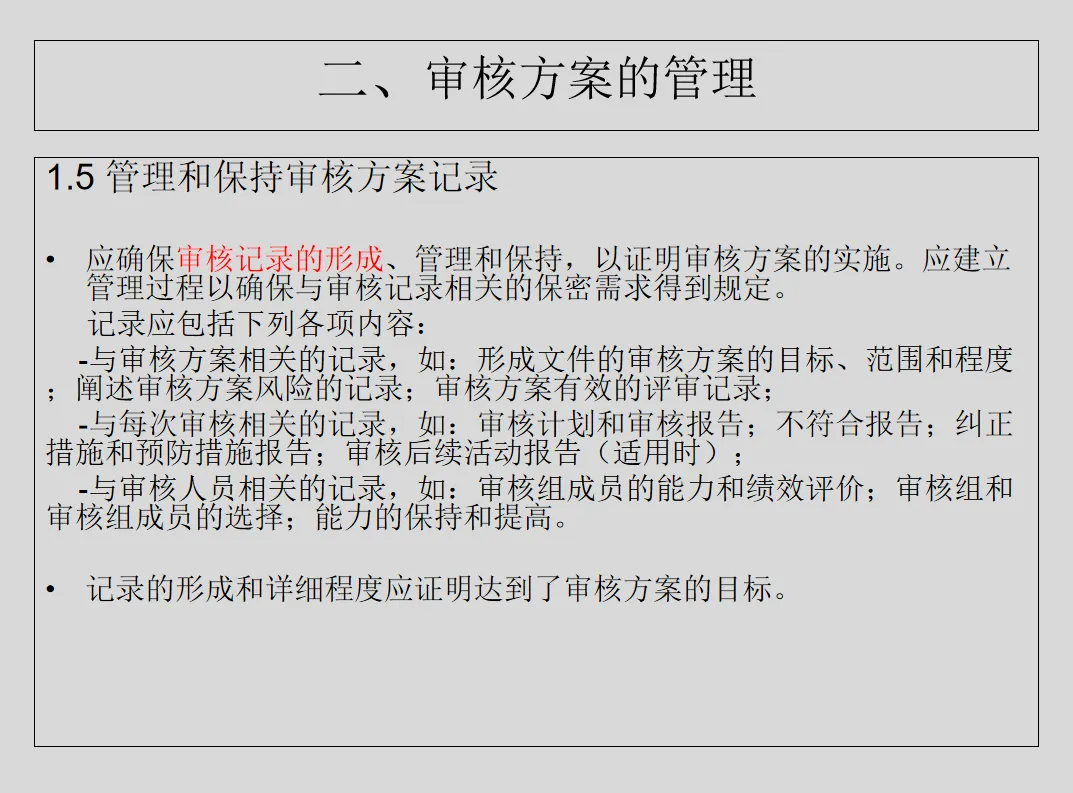
e) 保存记录,作为实施审核方案和审核结果的证据。
注:内部审核相关指南参见 GB/T 19011(ISO 19011, IDT)。
本次新要求取消了每年至少一次的规定,但是指南是规定至少12个月一次,并明确内部审核的周期和覆盖范围应当基于风险分析。
相关文件
(1)相关法律法规要求;如:《检验检测机构资质认定管理办法》(总局令第163号2021-4-2修订)、《检验检测机构监督管理办法》(总局令第 39号2025-3-18 总局令第 101 号修订);
(2)评审准则要求及特殊要求;
如:《检验检测机构资质认定评审准则》(2023)、GB/T 27025-2019《检测和校准实验室能力的通用要求》(ISO17025:2017、CNAS-CL01:2018)、行业特殊要求,及CNAS应用要求、应用说明等
(3)本机构管理体系文件
(4)检验检测标准和相关技术文件
(5)适用时,关注客户的要求
可参考:
GB/T 19011-2021《管理体系审核指南》、CNAS-GL011:2018《实验室和检验机构内部审核指南》




























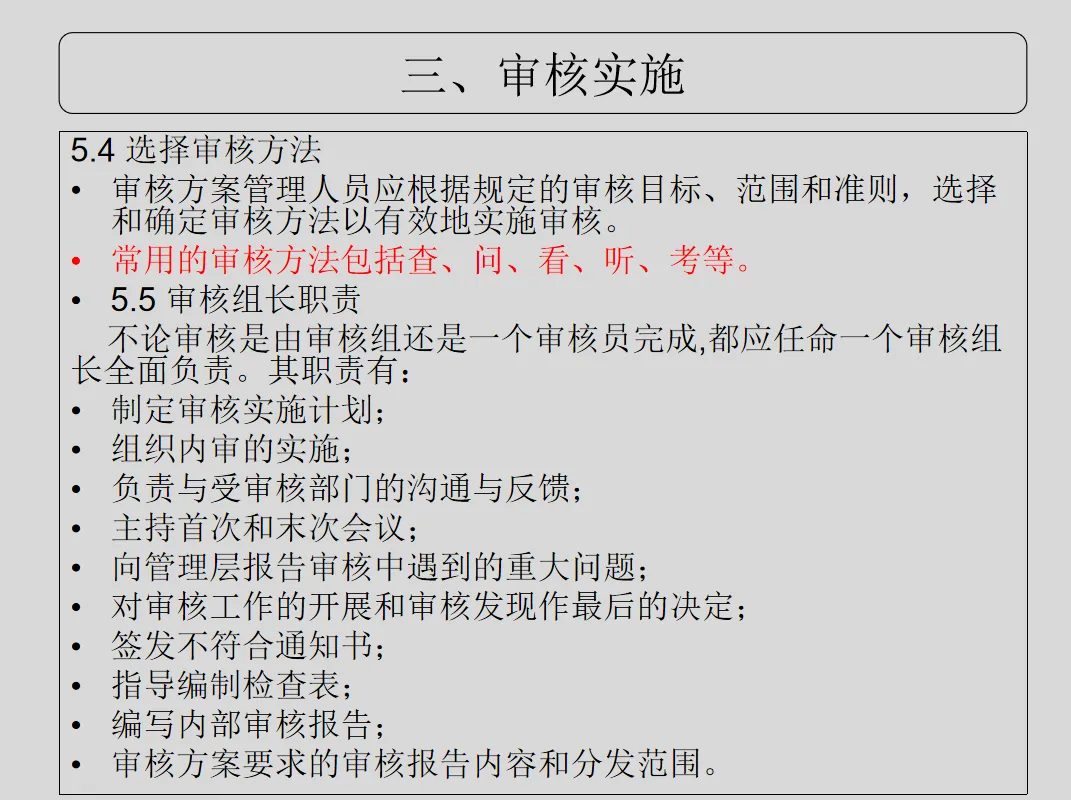
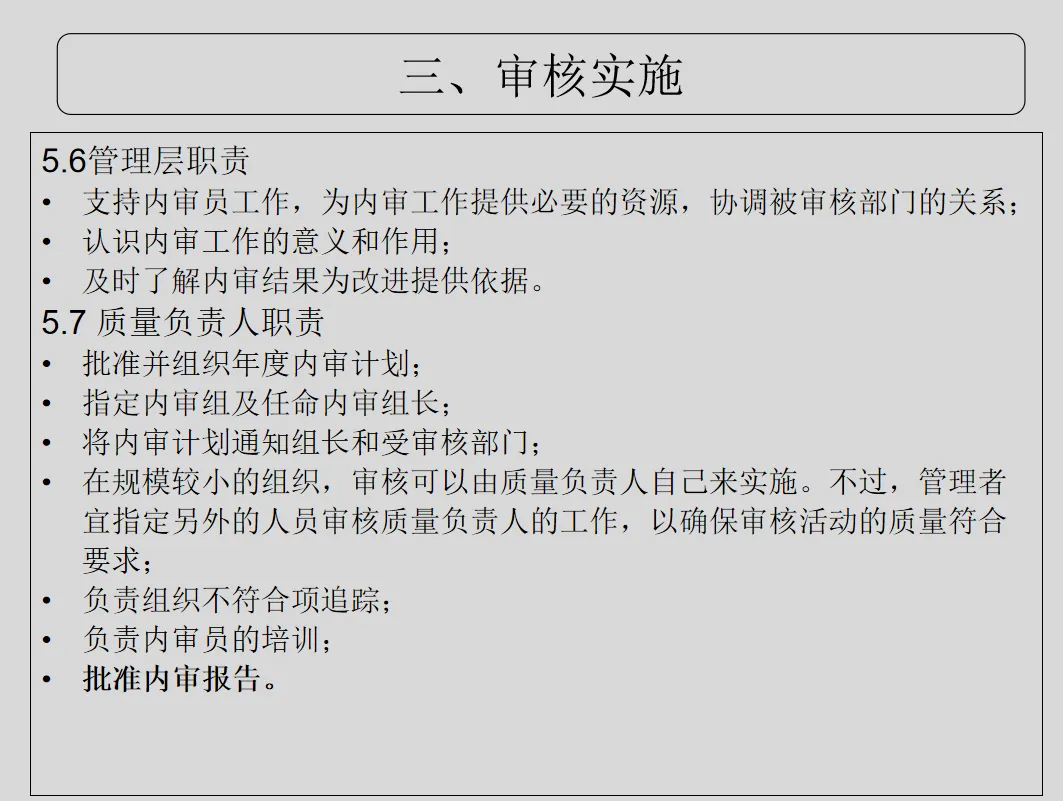
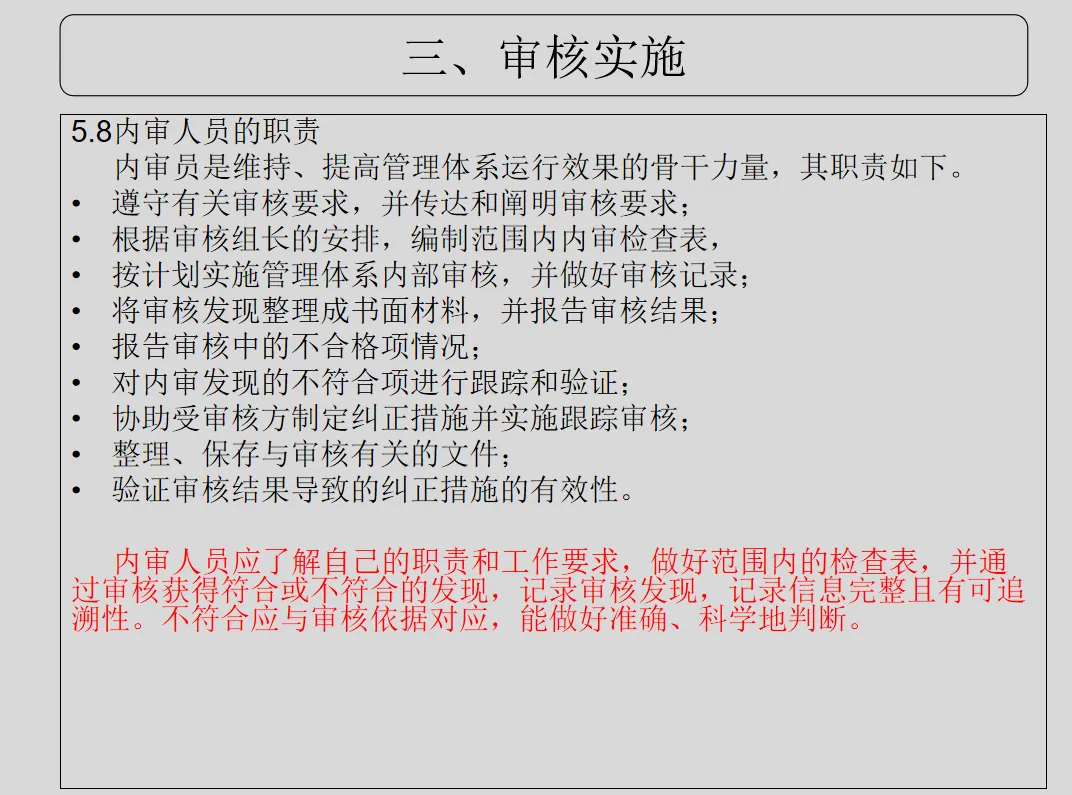

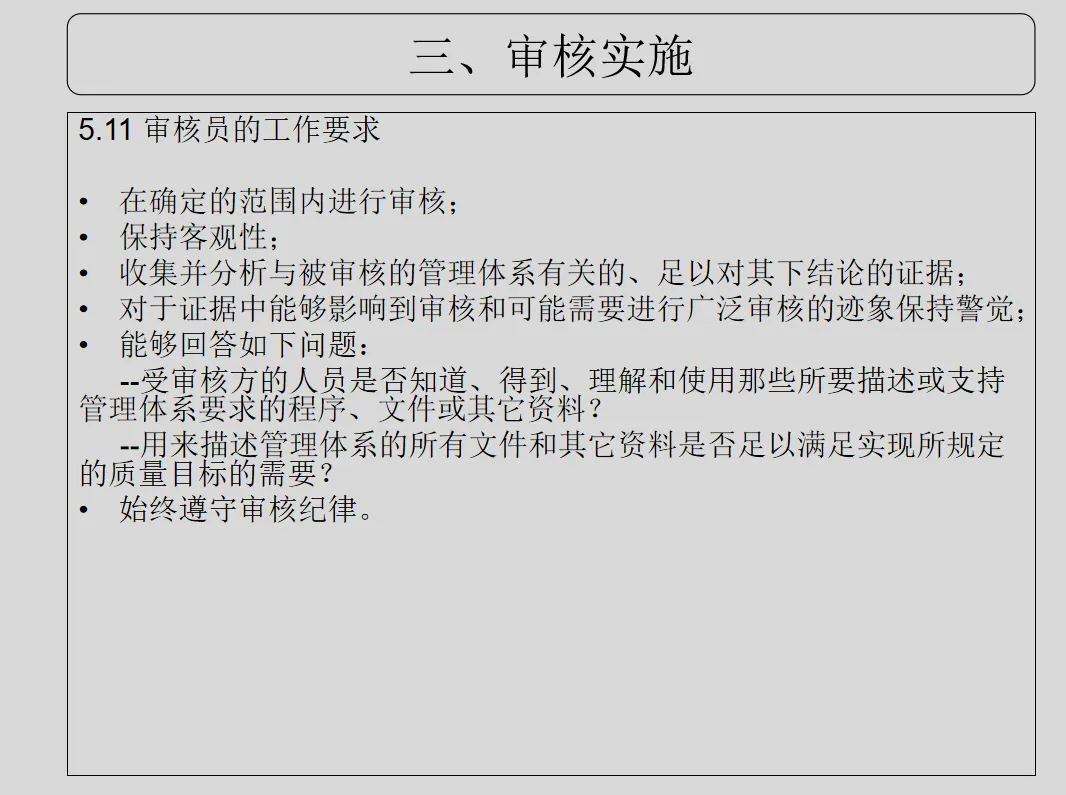
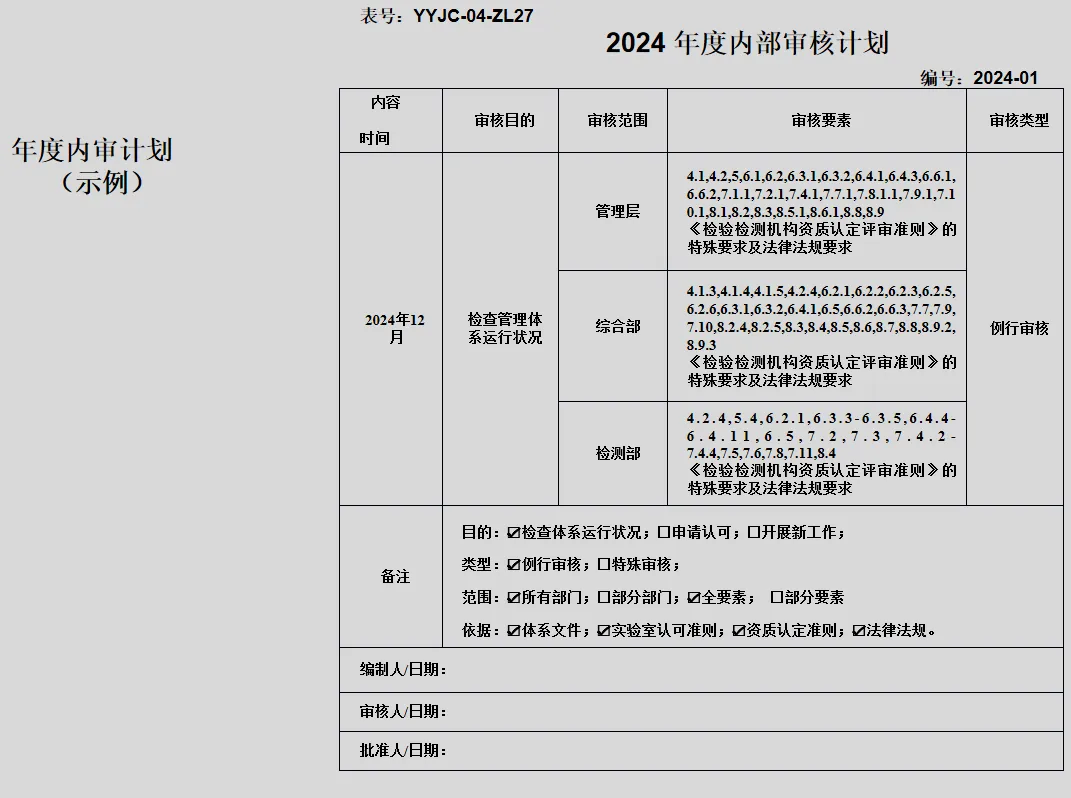


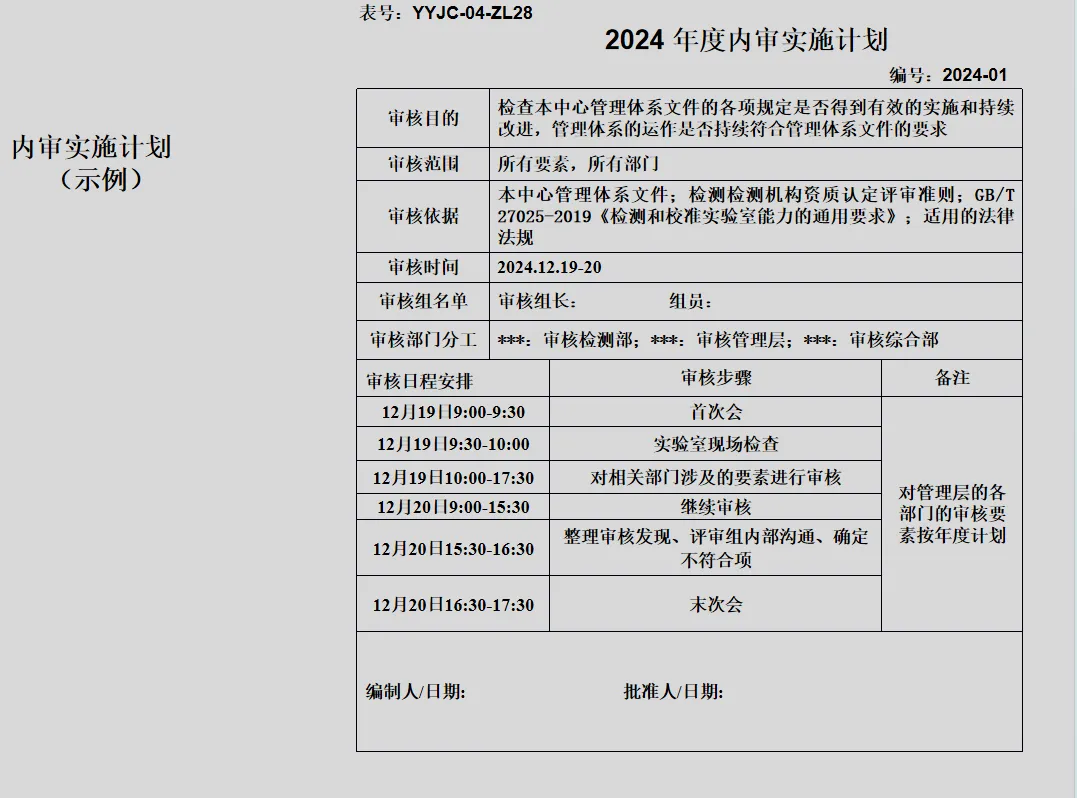





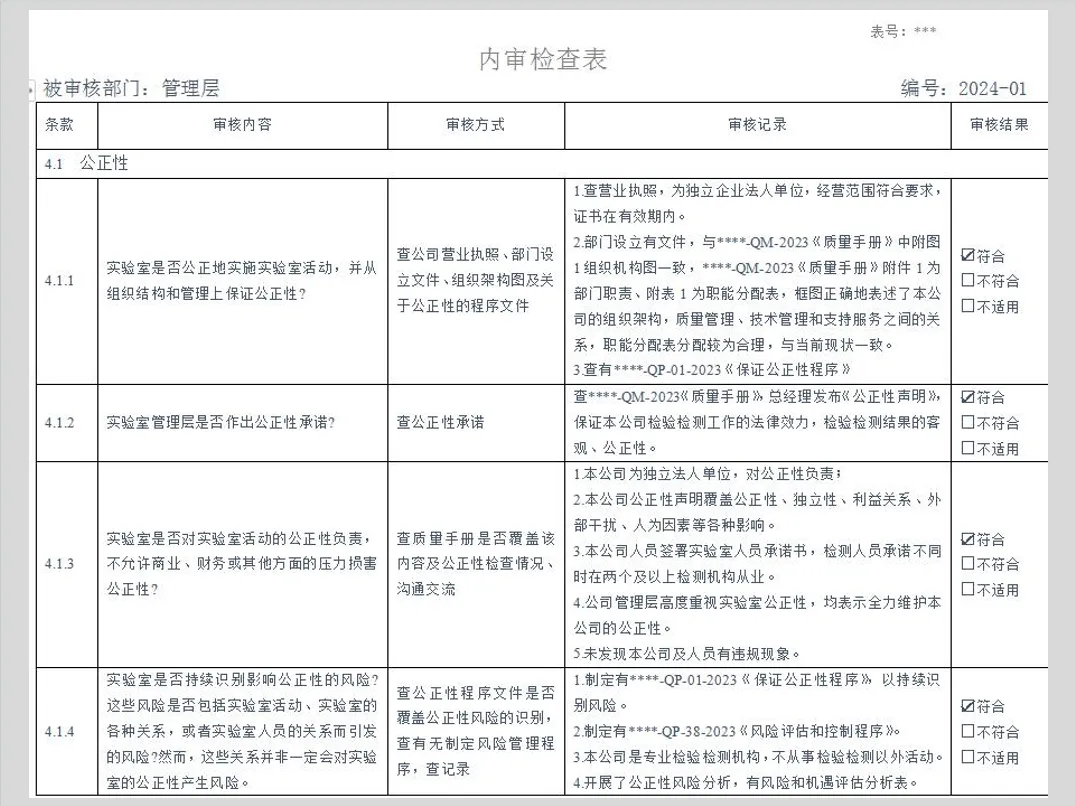
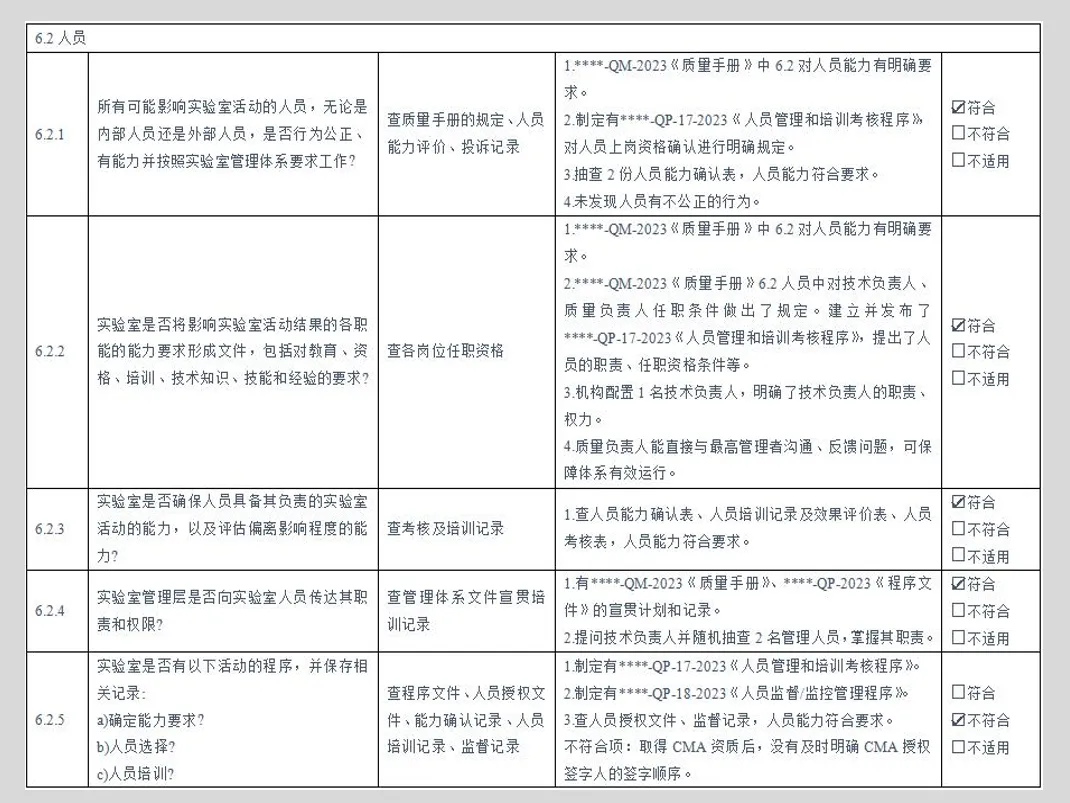








































































=8888

免责声明: 1. 本公众号发布的文章内容仅为信息分享、交流探讨之用,不构成任何专业建议,仅供读者参考。
2. 文章中涉及的观点仅代表作者个人,不代表本公众号立场,若内容存在事实错误或争议,欢迎读者指正。
3. 本公众号力求信息准确,但不对内容的完整性、及时性、有效性作任何承诺,因依赖本文信息导致的任何直接或间接损失,本公众号不承担责任。
