人教版高中化学必修第一册全册核心素养教案→文末下载
- 2026-04-19 16:47:21

绪言
第一章 物质及其变化
第一节 物质的分类及转化
第二节 离子反应
第三节 氧化还原反应
第二章 海水中的重要元素----钠和氯
第一节 钠及其化合物
第二节 氯及其化合物
第三节 物质的量
实验活动1 配制一定物质的量浓度的溶液
第三章 铁金属材料
第一节 铁及其化合物
第二节 金属材料
实验活动2 铁及其化合物的性质
第四章 物质结构元素周期律
第一节 原子结构与元素周期表
第二节 元素周期律
第三节 化学键
实验活动3 同周期、同主族元素性质的递变
全册核心素养教案
·绪言
一、教学目标
1.核心素养目标
o宏观辨识与微观探析:能从宏观层面认识化学研究的物质及其变化现象,从微观角度理解化学变化的本质是原子、分子层面的重新组合,建立宏观与微观相联系的思维方式。
o变化观念与平衡思想:认识化学变化是物质转化的基本形式,了解化学变化遵循一定规律,体会化学变化在创造物质、服务人类中的重要作用。
o证据推理与模型认知:通过化学发展历程中的重要史实,基于证据推理化学学科的发展逻辑,初步构建化学学习的基本模型。
o科学探究与创新意识:了解化学实验是化学研究的重要基础,激发对化学实验探究的兴趣,培养初步的科学探究意识和创新思维。
o科学态度与社会责任:认识化学学科在推动社会进步、解决资源、环境、健康等问题中的重要作用,树立可持续发展的观念和社会责任感。
2.知识与技能目标
o了解化学的定义、研究对象和研究内容。
o知晓化学发展的关键历程和重要里程碑。
o认识化学在现代社会中的应用领域和重要价值。
3.过程与方法目标
o通过阅读、分析、讨论等活动,培养获取和处理信息的能力。
o初步学会从不同角度认识化学学科,建立化学学习的基本思路。
4.情感态度与价值观目标
o激发对化学学科的学习兴趣和探究欲望。
o感受化学学科的魅力和化学工作者的科学精神。
二、教学重难点
1.教学重点:化学的定义和研究对象;化学在现代社会中的重要应用;化学核心素养的初步理解。
2.教学难点:宏观与微观相结合认识化学变化;化学核心素养在具体学习中的体现和应用。
三、教学方法
讲授法、讨论法、情境教学法、史料分析法
四、教学过程
(一)情境导入(5 分钟)
1.展示一组图片:古代陶瓷、青铜器、现代智能手机显示屏、污水处理厂、煤间接液化示范项目等。
2.提问:“这些物质和现象与什么学科密切相关?你对化学有哪些初步的认识?”
3.学生自由发言,分享对化学的初步印象。
4.教师总结:“这些物质的制备、转化和应用都离不开化学。化学是一门古老而又充满活力的学科,今天我们就一起走进化学的世界,开启高中化学的学习之旅。” 引出本节课主题 —— 绪言。
(二)新知探究(25 分钟)
1. 化学的定义与研究对象
·教师讲解:化学是在原子、分子水平上研究物质的组成、结构、性质、转化及其应用的基础自然科学。
·结合教材内容,从宏观和微观两个层面解析化学的研究对象:宏观上研究物质的性质、转化等现象;微观上探究物质的组成、结构等本质。
·提问:“结合生活实际,你能举例说明化学研究的内容吗?” 引导学生从身边的物质出发,如食物的消化、燃料的燃烧等,加深对化学研究对象的理解。
2. 化学的发展历程
·展示化学发展历程时间轴,介绍重要里程碑:波义耳提出科学的元素概念、拉瓦锡建立燃烧的氧化学说、道尔顿和阿伏加德罗提出原子 - 分子学说、门捷列夫发现元素周期律等。
·重点讲解我国化学史上的重要成就:侯德榜发明联合制碱法、人工合成结晶牛胰岛素和核糖核酸等,增强学生的民族自豪感。
·组织讨论:“从化学发展历程中,你能得到哪些启示?” 引导学生认识科学探究的艰辛、科学理论的不断完善等。
3. 化学的应用与价值
·分组讨论:“化学在现代社会的哪些领域发挥着重要作用?”
·各组代表发言后,教师总结化学在资源、材料、健康、环境等领域的应用:
o材料领域:金属材料、无机非金属材料、合成高分子材料等的研制。
o健康领域:药物的研发、食品添加剂的合理使用等。
o环境领域:污水处理、废气处理、新能源开发等。
·强调化学在推动社会可持续发展中的重要责任,树立学生的社会责任意识。
4. 化学学习的核心素养
·教师介绍高中化学核心素养的五个方面:宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知、科学探究与创新意识、科学态度与社会责任。
·结合本节课内容,举例说明核心素养的体现:如从宏观的物质变化现象联系微观的原子分子运动,体现宏观辨识与微观探析;从化学发展历程中基于证据得出科学结论,体现证据推理与模型认知等。
·引导学生认识核心素养对化学学习的指导意义,为后续学习奠定基础。
(三)课堂小结(5 分钟)
1.学生自主梳理本节课的核心知识点:化学的定义、研究对象、发展历程、应用价值和核心素养。
2.教师补充完善,强调重点内容,帮助学生构建知识框架。
(四)课堂练习(5 分钟)
1.化学是在( )水平上研究物质的组成、结构、性质、转化及其应用的基础自然科学。
A. 宏观 B. 微观 C. 原子、分子 D. 物质
答案:C
2.下列不属于化学研究范畴的是( )
A. 研发新能源 B. 合成新物质 C. 研究天体运动 D. 处理环境污染
答案:C
3.简述化学在现代社会中的重要应用(至少列举 3 个领域)。
答案:材料领域、健康领域、环境领域、资源利用领域等(合理即可)。
(五)布置作业(5 分钟)
1.查阅资料,了解一位你感兴趣的化学家的事迹,下节课分享交流。
2.思考:高中化学学习与初中化学学习有哪些不同?你打算如何学好高中化学?
3.预习第一章第一节 “物质的分类及转化”。
五、板书设计
绪言
1.化学的定义与研究对象
o定义:原子、分子水平研究物质的组成、结构、性质、转化及应用
o研究视角:宏观 + 微观
2.化学的发展历程
o重要里程碑:元素概念、氧化学说、原子 - 分子学说、元素周期律
o我国成就:侯氏制碱法、人工合成结晶牛胰岛素等
3.化学的应用与价值
o领域:资源、材料、健康、环境等
o责任:社会可持续发展
4.化学核心素养
o宏观辨识与微观探析
o变化观念与平衡思想
o证据推理与模型认知
o科学探究与创新意识
o科学态度与社会责任
六、教学反思
本节课通过情境导入、史料分析、讨论交流等多种教学方法,引导学生初步认识化学学科的定义、研究对象、发展历程和应用价值,同时渗透化学核心素养的培养。在教学过程中,应关注学生的已有知识基础和认知水平,充分调动学生的积极性和主动性。通过列举生活中的化学现象和我国化学史上的重要成就,有效激发了学生的学习兴趣和民族自豪感。但在核心素养的讲解过程中,可能过于抽象,需要在后续的具体章节学习中不断强化和渗透,帮助学生逐步理解和运用核心素养指导化学学习。
·第一章 物质及其变化
o第一节 物质的分类及转化
o第二节 离子反应
o第三节 氧化还原反应
第一章 物质及其变化 核心素养教案
一、章节核心素养目标
1.宏观辨识与微观探析:能从宏观视角对物质进行分类,辨识物质的转化类型(化合、分解、置换、复分解);能从微观角度(离子、电子转移)理解离子反应和氧化还原反应的本质,建立 “宏观现象 — 微观本质” 的关联。
2.变化观念与平衡思想:认识物质的转化是普遍存在的,且遵循一定规律(如质量守恒、电荷守恒);理解离子反应的发生条件,初步形成 “反应限度” 的意识(如离子共存、氧化还原反应的先后顺序)。
3.证据推理与模型认知:能基于实验现象或数据,推理物质的分类依据和转化规律;构建离子反应方程式、氧化还原反应 “双线桥” 等思维模型,用于解释和预测化学反应。
4.科学探究与创新意识:通过实验探究物质的分类标准、离子反应的发生条件、氧化还原反应的本质,培养实验设计、操作和分析能力;能基于已有知识,创新分类方法或探究方案。
5.科学态度与社会责任:认识物质分类和转化在生产、生活中的应用(如污水处理、金属冶炼),体会化学对人类社会的贡献;树立严谨求实的科学态度,重视化学规律的应用价值。
二、课时安排(共 8 课时)
内容板块 | 课时数 | 备注 |
第一节 物质的分类及转化 | 2 课时 | 含物质分类方法、物质转化类型与规律 |
第二节 离子反应 | 2 课时 | 含电解质与非电解质、离子反应方程式书写、离子共存 |
第三节 氧化还原反应 | 2 课时 | 含氧化还原反应判断、电子转移表示、氧化剂与还原剂 |
整理与提升 | 1 课时 | 知识体系构建、重难点突破 |
单元复习与检测 | 1 课时 | 素养评估与薄弱点巩固 |
三、分课时教学过程设计
第一节 物质的分类及转化(第 1 课时:物质的分类)
教学目标
1.掌握物质分类的基本方法(树状分类法、交叉分类法),能根据组成、性质对物质进行分类。
2.理解混合物、纯净物、单质、化合物、氧化物、酸、碱、盐的概念及相互关系。
3.培养分类思想,体会分类在化学研究和学习中的重要作用。
教学重难点
·重点:物质分类的基本方法,各类物质的概念及判断。
·难点:交叉分类法的应用,氧化物的分类(酸性、碱性、两性)。
教学过程
1.导入新课(5 分钟)
o展示图片:实验室药品柜、超市货架、图书馆书架的分类摆放场景,提问:“生活中为什么要对物品进行分类?化学研究中,成千上万种物质如何有序研究?”
o引出主题:物质的分类是化学研究的基础方法,通过分类可化繁为简、揭示物质的内在联系。
2.新课讲授:物质分类的基本方法(25 分钟)
o树状分类法
§定义:按照一定标准对物质进行层层分类,形成树状结构。
§核心标准:先根据组成物质的种类多少,分为混合物和纯净物;纯净物再根据组成元素种类,分为单质和化合物;化合物再根据性质或组成,分为氧化物、酸、碱、盐等。
§构建树状分类图(师生共同完成):
物质
├─ 混合物(多种物质组成,如空气、溶液、合金)
└─ 纯净物(一种物质组成)
├─ 单质(同种元素组成)
│├─ 金属单质(如Fe、Cu、Al)
│└─非金属单质(如O₂、C、H₂)
└─化合物(不同种元素组成)
├─ 氧化物(两种元素,其一为O)
│├─ 酸性氧化物(如CO₂、SO₂,能与碱反应生成盐和水)
│├─ 碱性氧化物(如CaO、Fe₂O₃,能与酸反应生成盐和水)
│└─两性氧化物(如Al₂O₃,既能与酸又能与碱反应生成盐和水)
├─ 酸(电离出的阳离子全为H⁺,如HCl、H₂SO₄、CH₃COOH)
├─ 碱(电离出的阴离子全为OH⁻,如NaOH、Ca(OH)₂)
└─盐(由金属阳离子或NH₄⁺与酸根阴离子组成,如NaCl、Na₂CO₃)
§实例分析:将下列物质分类 —— 空气(混合物)、Fe(金属单质)、O₂(非金属单质)、CO₂(酸性氧化物)、CaO(碱性氧化物)、HCl(酸)、NaOH(碱)、NaCl(盐)、Al₂O₃(两性氧化物)。
§强调:树状分类法的优点是层次清晰、标准统一,便于系统认识物质。
o交叉分类法
§定义:根据不同标准对同一物质进行分类,体现物质的多重属性。
§实例讲解:以 Na₂CO₃为例,从组成阳离子看,属于钠盐;从组成阴离子看,属于碳酸盐;从溶解性看,属于易溶性盐。
§表格呈现:对下列物质进行交叉分类
物质 | 按阳离子分类 | 按阴离子分类 | 按溶解性分类 |
Na₂CO₃ | 钠盐 | 碳酸盐 | 易溶盐 |
K₂SO₄ | 钾盐 | 硫酸盐 | 易溶盐 |
CaCO₃ | 钙盐 | 碳酸盐 | 难溶盐 |
NH₄Cl | 铵盐 | 盐酸盐 | 易溶盐 |
§小组讨论:“交叉分类法的优点是什么?”(结论:能全面、多角度认识物质的性质和类别)
o氧化物的分类与性质(重点突破)
§演示实验:
1.取少量 CaO 粉末于试管中,加入适量稀盐酸,观察到粉末溶解,溶液澄清(证明碱性氧化物与酸反应),反应方程式:
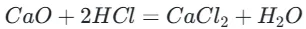
2.取少量 CO₂气体通入澄清石灰水,观察到石灰水变浑浊(证明酸性氧化物与碱反应),反应方程式:。
3.(可选)取少量 Al₂O₃粉末,分别加入稀盐酸和 NaOH 溶液,观察到均溶解(证明两性氧化物的性质),反应方程式:、
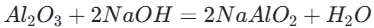
§总结:酸性氧化物≠非金属氧化物(如 Mn₂O₇是酸性氧化物),碱性氧化物≠金属氧化物(如 Al₂O₃是两性氧化物)。
3.新课讲授:分类方法的应用(10 分钟)
o化学研究中的应用:通过分类,可预测物质的性质(如知道某物质是酸性氧化物,可预测其能与碱反应);便于寻找具有相似性质的物质(如研究盐的性质时,可选择 NaCl、Na₂CO₃等典型盐作为代表)。
o生活中的应用:如垃圾分类(可回收物、厨余垃圾、有害垃圾),便于资源回收和环境治理;药品分类(处方药、非处方药),便于安全使用。
o拓展思考:“如何根据物质的性质设计新的分类标准?”(如按物质的状态分为固态、液态、气态;按物质的导电性分为导体、半导体、绝缘体)。
4.课堂小结与练习(5 分钟)
o小结:物质分类的两种核心方法(树状分类法、交叉分类法),各类物质的概念及关系,分类的重要意义。
o练习:下列说法正确的是( )
A. 含有氧元素的化合物一定是氧化物 B. 酸电离出的阳离子全为 H⁺ C. 盐一定由金属阳离子和酸根阴离子组成 D. 碱性氧化物一定是金属氧化物(答案:BD)
板书设计
一、物质的分类
1. 树状分类法(层次清晰)
物质→混合物/纯净物→单质(金属/非金属)/化合物
化合物→氧化物(酸性/碱性/两性)、酸、碱、盐
2. 交叉分类法(多角度认识)
例:Na₂CO₃→钠盐、碳酸盐、易溶盐
3. 氧化物分类与性质
-酸性氧化物:与碱反应生成盐和水(CO₂、SO₂)
-碱性氧化物:与酸反应生成盐和水(CaO、Fe₂O₃)
-两性氧化物:与酸、碱均反应(Al₂O₃)
4. 分类的应用:预测性质、便于研究、生活实用
第一节 物质的分类及转化(第 2 课时:物质的转化)
教学目标
1.认识常见物质的转化类型(化合、分解、置换、复分解反应),能书写相关化学方程式。
2.理解物质转化的规律,掌握各类物质(单质、氧化物、酸、碱、盐)之间的转化关系。
3.能根据物质转化规律设计简单的物质制备方案,培养应用能力。
教学重难点
·重点:物质转化的四种基本反应类型,各类物质之间的转化关系。
·难点:利用转化规律设计物质制备方案,反应条件对转化的影响。
教学过程
1.复习导入(5 分钟)
o回顾上节课物质分类的方法,提问:“不同类别的物质之间能否相互转化?如铁如何转化为铁锈?盐酸如何转化为氯化钠?”
o展示物质转化实例图片:铁生锈、石灰石煅烧、酸碱中和,引出本节课主题 —— 物质的转化。
2.新课讲授:物质转化的基本反应类型(20 分钟)
o梳理四种基本反应类型的定义、特点及实例:
i.化合反应
·定义:由两种或两种以上物质生成一种物质的反应(A + B → AB)。
·特点:“多变一”。
·实例:
o金属与氧气反应:;
o非金属与氧气反应:;
o氧化物与水反应:
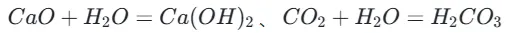
·强调:并非所有氧化物都能与水反应(如 Fe₂O₃、SiO₂不溶于水,也不与水反应)。
ii.分解反应
·定义:由一种物质生成两种或两种以上物质的反应(AB → A + B)。
·特点:“一变多”。
·实例:
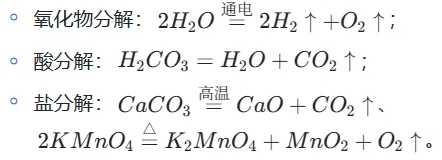
iii.置换反应
·定义:一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应(A + BC → AC + B)。
·特点:“单换单”,一定有元素化合价变化。
·实例:
o金属与酸反应:;
o金属与盐溶液反应:(强调:活泼金属置换不活泼金属,需符合金属活动性顺序);
o非金属与金属氧化物反应。
iv.复分解反应
定义:两种化合物相互交换成分,生成另外两种化合
可长按扫码下载完整电子版
▼ 
电脑端下载网址 https://jazpan.com/box/371.html
可长按扫码下载完整电子版

 点击阅读原文下载完整电子版打印资料
点击阅读原文下载完整电子版打印资料
