鲁科版高中化学必修第2册全册核心素养教案→文末下载(鲁教版)
- 2026-04-21 06:07:51


| 一年级 | 二年级 | 三年级 | 四年级 | 五年级 |
| 六年级 | 七年级 | 八年级 | 九年级 | 高中 |
| 语文 | 数学 | 英语 | 科学 | 道政 |
| 物理 | 化学 | 历史 | 地理 | 生物 |
| 美术 | 音乐 | 综实 | 劳动 | 信息 |
| 体健 | 心理 | 地方 | 思政 | 汇总 |

第 1 章 原子结构 元素周期律 第 1 节 原子结构与元素性质 第 2 节 元素周期律和元素周期表 第 3 节 元素周期表的应用 微项目 海带提碘与海水提溴 —— 体验元素性质递变规律的实际应用 本章自我评价
第 2 章 化学键 化学反应规律 第 1 节 化学键与物质构成 第 2 节 化学反应与能量转化 第 3 节 化学反应的快慢和限度 微项目 研究车用燃料及安全气囊 —— 利用化学反应解决实际问题 本章自我评价
第 3 章 简单的有机化合物 第 1 节 认识有机化合物 第 2 节 从化石燃料中获取有机化合物 第 3 节 饮食中的有机化合物 微项目 自制米酒 —— 领略我国传统酿造工艺的魅力 本章自我评价 附录
1. 各章节中的主要术语与物质名称 2. 本册教材中主要的实验内容 3. 常见元素中英文名称对照表 4. 部分酸、碱和盐的溶解性表(室温)
鲁科版高中化学选修第1册《化学反应原理》全册核素教案 鲁科版高中化学选修第2册《物质结构与性质》全册核素教案 鲁科版高中化学选修第3册《有机化学基础》全册核心素养教案 高中资料汇总:核心素养教案+课件+知识点+试卷+大单元设计+计划 全册核心素养教案
·第 1 章 原子结构 元素周期律
o第 1 节 原子结构与元素性质
o第 2 节 元素周期律和元素周期表
o第 3 节 元素周期表的应用
o微项目 海带提碘与海水提溴 —— 体验元素性质递变规律的实际应用
o本章自我评价
鲁科版高中化学必修第二册第1章核心素养教案
一、本章课时安排
本章共设置8课时,具体分配如下:
·第1节 原子结构与元素性质:2课时
·第2节 元素周期律和元素周期表:2课时
·第3节 元素周期表的应用:2课时
·微项目 海带提碘与海水提溴:1课时
·本章自我评价:1课时
二、本章核心素养目标
1.宏观辨识与微观探析:能从宏观元素性质递变现象,探析原子结构(质子数、电子层数、最外层电子数)的微观本质,建立“结构决定性质”的认知模型。
2.证据推理与模型认知:通过分析实验数据、原子结构信息,推理元素周期律的本质;能运用元素周期表模型预测元素性质及化合物的化学性质。
3.科学探究与创新意识:参与元素性质递变、海带提碘等探究实验,体验科学探究的基本流程;能基于探究结果创新实验方案或优化物质提取流程。
4.科学态度与社会责任:认识元素周期律对化学研究、工业生产的指导价值;体会海水资源利用的意义,强化可持续发展意识和社会责任。
三、分节详细教案
第1节 原子结构与元素性质(第1课时:原子结构、核素与同位素)
教学目标
1.掌握原子的构成(原子核、质子、中子、电子)及各微粒间的数量关系。
2.理解质量数、核素、同位素的概念,能规范表示原子符号。
3.建立“原子结构决定元素种类、核素种类”的认知。
教学重难点
·重点:原子构成微粒的数量关系、核素与同位素的概念。
·难点:同位素的应用及元素相对原子质量的计算逻辑。
教学过程
1.情境导入(5分钟)展示卢瑟福α粒子散射实验示意图,提问:“实验中绝大多数α粒子穿过金箔,少数偏转,个别反弹,这一现象能说明原子的什么结构特点?”引导学生回顾初中原子结构知识,引出本节课核心问题:“原子的内部结构究竟是怎样的?各微粒之间有什么关系?”
2.新知探究一:原子的构成(15分钟)呈现电子、质子、中子的基本数据表(质量、相对质量、电量、电荷),组织学生小组讨论:学生汇报讨论结果,教师总结并板书核心关系式:即时练习:写出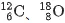 的质子数、中子数、核外电子数,巩固微粒数量关系。
的质子数、中子数、核外电子数,巩固微粒数量关系。
1.原子中质子数、核电荷数、核外电子数的关系及原因。
2.原子的质量主要由哪些微粒决定?
3.忽略电子质量时,原子相对质量与质子数、中子数的关系。
4.核电荷数 = 质子数 = 核外电子数
5.质量数(A)= 质子数(Z)+ 中子数(N)
6.原子符号表示:$\ce{_{Z}^{A}X}$(X为元素符号)
3.新知探究二:核素与同位素(15分钟)展示氕、氘、氚的原子结构示意图及相关信息(俗称、发现年份),提问:“这三种粒子的质子数、中子数、电子数有何异同?它们属于同一种元素吗?”引出核素概念:具有相同质子数和相同中子数的一类原子。进一步引导:“氕、氘、氚的质子数相同,中子数不同,它们之间是什么关系?”给出同位素定义:质子数相同而中子数不同的同一种元素的不同核素互为同位素。举例说明同位素的应用: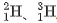 用于制造氢弹;
用于制造氢弹;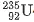 作为核反应堆燃料;放射性同位素用于示踪、探伤、医疗诊断等。补充元素相对原子质量的计算方法:各核素相对原子质量与丰度的乘积之和,结合氯元素两种核素
作为核反应堆燃料;放射性同位素用于示踪、探伤、医疗诊断等。补充元素相对原子质量的计算方法:各核素相对原子质量与丰度的乘积之和,结合氯元素两种核素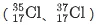 的丰度数据,演示计算过程。
的丰度数据,演示计算过程。
4.课堂小结与巩固(5分钟)梳理本节课核心知识点:原子构成→微粒关系→核素→同位素。课堂练习:判断下列说法是否正确:布置作业:查阅资料,了解一种放射性同位素的具体应用场景。
1.同种元素的不同核素化学性质完全相同(正确,质子数相同,最外层电子数相同)。
2.质子数相同的粒子一定是同种元素(错误,如$\ce{NH_{4}^{+}}$与$\ce{Na^{+}}$)。
第1节 原子结构与元素性质(第2课时:核外电子排布与元素性质)
教学目标
1.掌握核外电子分层排布的规律,能绘制核电荷数1-20号元素的原子结构示意图。
2.理解原子最外层电子数与元素得失电子能力、化合价的关系。
3.初步建立“电子排布决定元素化学性质”的认知模型。
教学重难点
·重点:核外电子排布规律、原子结构示意图的绘制。
·难点:原子结构与元素得失电子能力、化合价的关联。
教学过程
1.复习导入(5分钟)回顾上节课知识点:原子符号$\ce{_{Z}^{A}X}$的含义、同位素概念。提问:“同种元素的原子化学性质是否完全相同?为什么?”引出核外电子排布的重要性。
2.新知探究一:核外电子排布规律(15分钟)讲解核外电子分层排布的理论依据:能量低的电子离核近,能量高的电子离核远,电子层分为K、L、M、N、O、P、Q层(对应n=1-7)。呈现核外电子排布的核心规律:示范绘制钠原子($\ce{Na}$,核电荷数11)、氯原子($\ce{Cl}$,核电荷数17)的原子结构示意图,强调圆圈、弧线、数字的含义。学生分组练习:绘制核电荷数1-20号元素的原子结构示意图,小组内互相检查纠错,教师巡视指导。
1.各电子层最多容纳$2n^2$个电子(n为电子层数)。
2.最外层电子数不超过8个(K层为最外层时不超过2个)。
3.电子优先排布在能量较低的电子层,填满后再排布到能量较高的电子层。
3.新知探究二:原子结构与元素性质(15分钟)呈现稀有气体、金属、非金属元素的原子最外层电子数特点,组织学生讨论:总结规律:举例验证:钠原子(最外层1个电子)易失1个电子,呈+1价;氯原子(最外层7个电子)易得1个电子,呈-1价;氧原子(最外层6个电子)易得2个电子,呈-2价。拓展视野:介绍玻尔原子模型和电子云模型,说明核外电子运动的特殊性(无固定轨迹,仅能描述概率分布),加深学生对电子排布的理解。
1.稀有气体元素原子最外层电子数为8(氦为2),化学性质稳定,原因是什么?
2.金属元素原子最外层电子数一般小于4,非金属元素原子最外层电子数一般大于或等于4,这与它们的得失电子能力有何关系?
3.稀有气体元素:原子结构稳定,不易得失电子,化合价为0。
4.金属元素:易失去最外层电子形成阳离子,化合价为正价(数值等于失去的电子数)。
5.非金属元素:易得到电子形成阴离子,化合价为负价(数值等于得到的电子数)。
4.课堂小结与巩固(5分钟)梳理核心逻辑:电子分层排布→最外层电子数特点→元素得失电子能力→化合价。课堂练习:布置作业:结合原子结构示意图,分析第3周期元素原子得失电子能力的变化趋势。
1.下列原子结构示意图是否正确?若错误请改正:$\ce{Mg}$(+12 2 8 2)、$\ce{Si}$(+14 2 9 3)。
2.分析铝原子($\ce{Al}$)的最外层电子数,预测其得失电子能力及常见化合价。
第2节 元素周期律和元素周期表(第1课时:元素周期律)
教学目标
1.通过分析数据,探究原子序数递增时元素原子最外层电子数、原子半径、化合价的周期性变化。
2.理解元素周期律的含义及实质。
3.提升数据分析、归纳总结的科学探究能力。
教学重难点
·重点:元素周期律的具体表现(最外层电子数、原子半径、化合价的周期性变化)。
·难点:元素周期律的实质(原子核外电子排布的周期性变化)。
教学过程
1.情境导入(5分钟)展示元素周期表图片,提问:“目前已发现的110多种元素,为何能按照一定规律排列在周期表中?它们的性质之间存在怎样的内在联系?”引出本节课主题:元素性质随原子序数的递增是否存在规律性变化?
2.新知探究:元素周期律的探究(25分钟)呈现原子序数1-18号元素的相关数据(电子层数、最外层电子数、原子半径、常见化合价),组织学生进行分组探究:学生汇报探究结果,教师引导总结:引出元素周期律的定义:元素的性质随着元素原子序数的递增而呈周期性变化。深入分析实质:元素性质的周期性变化是原子核外电子排布周期性变化的必然结果(同周期元素电子层数相同,最外层电子数递增;同主族元素最外层电子数相同,电子层数递增)。拓展视野:介绍人类对元素周期律的认识历程(门捷列夫基于原子量的早期认识→莫斯莱基于核电荷数的修正→现代基于核外电子排布的本质认知),体现科学探究的渐进性。
1.以原子序数为横坐标,最外层电子数为纵坐标绘制柱状图,观察变化规律。
2.分析原子半径数据,总结同周期、同主族元素原子半径的变化趋势。
3.梳理各元素的常见化合价,找出化合价与最外层电子数的关系及变化规律。
4.最外层电子数:随原子序数递增,从1递增到8(第一周期除外),呈现周期性变化。
5.原子半径:同周期从左到右逐渐减小,同主族从上到下逐渐增大,呈现周期性变化。
6.化合价:正价从+1递增到+7(O、F除外),负价从-4递增到-1,呈现周期性变化。
3.课堂小结与巩固(10分钟)梳理探究流程:数据收集→图表分析→规律总结→揭示实质。课堂练习:布置作业:查阅资料,了解元素周期律在预测未知元素性质中的应用实例。
1.下列关于元素性质递变的说法错误的是( )
2.分析第2周期元素从$\ce{Li}$到$\ce{F}$的性质递变,说明其与核外电子排布的关系。
第2节 元素周期律和元素周期表(第2课时:元素周期表)
教学目标
1.掌握元素周期表的结构(周期、族的划分及特点)。
2.理解元素在周期表中的位置与原子结构的关系。
3.认识主族元素、副族元素、过渡元素、稀土元素的特点。
教学重难点
·重点:元素周期表的结构(周期、族的分类及数量)。
·难点:元素位置与原子结构(电子层数、最外层电子数)的关联。
教学过程
1.复习导入(5分钟)回顾元素周期律的核心内容及实质。提问:“元素周期律是通过什么载体直观呈现的?元素周期表的结构如何体现元素周期律?”引出本节课主题。
2.新知探究一:元素周期表的周期结构(10分钟)展示元素周期表,讲解周期的定义:元素周期表中的横行称为周期,周期序数等于该周期元素原子的电子层数。分析周期的分类及特点:强调:除第1周期外,每个周期都从最外层电子数为1的金属元素开始,过渡到最外层电子数为7的非金属元素,最后以最外层电子数为8的稀有气体元素结束。
1.短周期(1、2、3周期):分别含2、8、8种元素,电子层数依次为1、2、3。
2.长周期(4、5、6、7周期):分别含18、18、32、32种元素(第7周期为不完全周期,已发现所有元素),电子层数依次为4、5、6、7。
3.新知探究二:元素周期表的族结构(15分钟)讲解族的定义:元素周期表中的纵列称为族,共18个纵列,16个族。分类说明:举例说明:钠元素($\ce{Na}$)位于第3周期ⅠA族,电子层数3,最外层电子数1;氯元素($\ce{Cl}$)位于第3周期ⅦA族,电子层数3,最外层电子数7;碳元素($\ce{C}$)位于第2周期ⅣA族,电子层数2,最外层电子数4。拓展介绍:镧系元素(第6周期57-71号元素)、锕系元素(第7周期89-103号元素)的特点(原子结构相似、化学性质相近),及稀土元素的定义(ⅢB族钪、钇和镧系元素的统称)和应用价值。
1.主族(A族):由短周期和长周期元素组成,共7个主族(ⅠA-ⅦA),族序数等于最外层电子数。
2.副族(B族):仅由长周期元素组成,共7个副族(ⅠB-ⅦB)。
3.Ⅷ族:第8、9、10三个纵列,共1个族。
4.0族:第18纵列,由稀有气体元素组成,最外层电子数为8(氦为2),化学性质稳定。
4.新知探究三:元素周期表与原子结构的关系(5分钟)总结核心关联:学生练习:根据原子结构示意图判断元素在周期表中的位置,或根据元素位置推断原子结构。
1.周期序数 = 电子层数
2.主族序数 = 最外层电子数
3.原子序数 = 质子数 = 核电荷数 = 核外电子数
5.课堂小结与巩固(5分钟)梳理元素周期表结构:7个周期(3短4长)、16个族(7主7副1Ⅷ10)。课堂练习:布置作业:绘制元素周期表的结构示意图(标注周期、族的分类及数量)。
1.指出下列元素在周期表中的位置:$\ce{K}$(第4周期ⅠA族)、$\ce{Br}$(第4周期ⅦA族)、$\ce{Ar}$(第3周期0族)。
2.某元素位于第3周期ⅤA族,该元素的原子最外层电子数为______,电子层数为______,原子序数为______。
第3节 元素周期表的应用(第1课时:同周期、同主族元素性质递变)
教学目标
1.掌握同周期、同主族元素原子得失电子能力的递变规律。
2.学会通过实验或资料分析验证元素性质递变规律。
3.提升实验设计、证据推理的能力。
教学重难点
·重点:同周期(从左到右)、同主族(从上到下)元素得失电子能力的递变规律。
·难点:元素性质递变规律的实验验证与本质解释。
教学过程
1.复习导入(5分钟)回顾元素周期表的结构及原子结构与元素位置的关系。提问:“同周期、同主族元素的原子结构存在规律性变化,那么它们的化学性质(得失电子能力)会如何变化?如何验证这种变化?”
2.新知探究一:同周期元素性质递变(15分钟)明确研究对象:第3周期元素($\ce{Na}$、$\ce{Mg}$、$\ce{Al}$、$\ce{Si}$、$\ce{P}$、$\ce{S}$、$\ce{Cl}$)。提出问题:第3周期元素从左到右,原子失电子能力、得电子能力如何变化?实验探究(学生必做实验):比较钠、镁、铝的失电子能力。实验用品:金属钠(小块)、镁条、铝片、蒸馏水、酚酞溶液、烧杯、试管、镊子、砂纸。实验步骤:小组讨论:资料补充:展示$\ce{Si}$、$\ce{P}$、$\ce{S}$、$\ce{Cl}$与氢气反应的条件及氢化物稳定性数据:$\ce{SiH_{4}}$需高温下反应且不稳定,$\ce{PH_{3}}$加热易分解,$\ce{H_{2}S}$受热分解,$\ce{HCl}$稳定难分解。引导学生分析:同周期从左到右,非金属元素得电子能力逐渐增强(与氢气反应难度降低,氢化物稳定性增强)。
1.取3支试管,分别加入少量蒸馏水,滴加2滴酚酞溶液。
2.用镊子取一小块钠,吸干表面煤油后放入第一支试管,观察现象(钠浮在水面、剧烈反应、产生大量气泡、溶液变红),记录反应剧烈程度。
3.取一段镁条,用砂纸打磨去除氧化膜,放入第二支试管,观察现象(缓慢产生气泡,溶液微弱变红);加热试管,观察现象变化(反应加快,气泡增多,溶液红色加深)。
4.取一片铝片,用砂纸打磨去除氧化膜,放入第三支试管,观察现象(无明显气泡产生);加热试管,仍无明显气泡。
5.钠、镁、铝与水反应的剧烈程度排序:钠 > 镁(加热)> 铝(加热无明显现象),该现象说明三者失电子能力如何变化?(失电子能力:$\ce{Na}$ > $\ce{Mg}$ > $\ce{Al}$)
6.结合原子结构分析原因:同周期元素电子层数相同,从左到右质子数递增,原子核对最外层电子的吸引力增强,失电子能力逐渐减弱。
3.新知探究二:同主族元素性质递变(15分钟)明确研究对象:第ⅠA族($\ce{Li}$、$\ce{Na}$、$\ce{K}$)和第ⅦA族($\ce{F}$、$\ce{Cl}$、$\ce{Br}$、$\ce{I}$)元素。实验探究(演示实验):比较钠、钾的失电子能力。实验操作:分别取小块钠、钾,吸干煤油后放入盛有冷水的烧杯中,观察反应剧烈程度(钾与水反应比钠更剧烈,产生的氢气燃烧,并有轻微爆炸)。结论:第ⅠA族元素从上到下,失电子能力逐渐增强($\ce{Li}$ < $\ce{Na}$ < $\ce{K}$)。资料探究:分析第ⅦA族元素性质数据(单质氧化性、氢化物稳定性、置换反应):小组讨论:结合原子结构分析同主族元素性质递变原因:同主族元素最外层电子数相同,从上到下电子层数递增,原子核对最外层电子的吸引力减弱,失电子能力逐渐增强,得电子能力逐渐减弱。
1.氧化性:$\ce{F_{2}}$ > $\ce{Cl_{2}}$ > $\ce{Br_{2}}$ > $\ce{I_{2}}$(如$\ce{Cl_{2}}$能置换$\ce{NaBr}$溶液中的$\ce{Br_{2}}$,$\ce{Br_{2}}$能置换$\ce{KI}$溶液中的$\ce{I_{2}}$)。
2.氢化物稳定性:$\ce{HF}$ > $\ce{HCl}$ > $\ce{HBr}$ > $\ce{HI}$。
4.课堂小结与巩固(5分钟)总结递变规律:课堂练习:判断下列说法是否正确:布置作业:设计实验方案,验证第2周期元素$\ce{Li}$、$\ce{Be}$的失电子能力强弱。
1.同周期(左→右):失电子能力减弱,得电子能力增强;金属性减弱,非金属性增强。
2.同主族(上→下):失电子能力增强,得电子能力减弱;金属性增强,非金属性减弱。
3.第3周期元素从$\ce{Na}$到$\ce{Cl}$,金属性逐渐增强(错误)。
4.第ⅦA族元素从上到下,得电子能力逐渐减弱,氢化物稳定性逐渐降低(正确)。
第3节 元素周期表的应用(第2课时:元素周期表的实际应用)
教学目标
1.学会运用元素周期表预测未知元素的性质。
2.理解元素周期表在寻找新材料、指导化学研究等领域的应用价值。
3.强化“结构决定性质,性质决定用途”的化学观念。
教学重难点
·重点:元素周期表在预测元素性质、寻找新材料中的应用。
·难点:基于元素周期表的性质预测逻辑与应用。
教学过程
1.复习导入(5分钟)回顾同周期、同主族元素性质递变规律。提问:“掌握元素周期律和元素周期表的知识,能帮助我们解决哪些实际问题?科学家是如何利用元素周期表推动化学研究的?”引出本节课主题。
2.新知探究一:预测未知元素的性质(15分钟)案例分析:以第4周期ⅣA族元素锗($\ce{Ge}$)为例,预测其性质。引导学生思考:资料验证:展示锗的实际性质(半导体材料、$\ce{H_{2}GeO_{3}}$为弱酸、能与盐酸和强碱反应),验证预测的合理性。方法总结:预测未知元素性质的思路——先确定元素在周期表中的位置→找出相邻(同周期、同主族)已知元素→依据递变规律推测性质。学生练习:预测第5周期ⅥA族元素碲($\ce{Te}$)的最高价氧化物对应水化物的酸性强弱,及与氢气反应的难易程度。
1.锗在周期表中的位置:第4周期ⅣA族,相邻元素为硅($\ce{Si}$,上方)、锡($\ce{Sn}$,下方)、镓($\ce{Ga}$,左方)、砷($\ce{As}$,右方)。
2.依据同主族性质递变:硅是非金属,锡是金属,推测锗可能是半导体;硅的最高价氧化物对应水化物($\ce{H_{2}SiO_{3}}$)是弱酸,推测锗的最高价氧化物对应水化物($\ce{H_{2}GeO_{3}}$)也为弱酸,且酸性弱于$\ce{H_{2}SiO_{3}}$。
3.依据同周期性质递变:左方镓是金属,右方砷是非金属,进一步佐证锗的金属性弱于镓,非金属性弱于砷。
3.新知探究二:元素周期表在寻找新材料中的应用(15分钟)分类讲解应用场景:视频拓展:播放“元素周期表与新材料研发”短视频,展示周期表在新能源、新材料领域的最新应用,增强学生的直观认知。
1.寻找半导体材料:在金属与非金属的分界线附近(如$\ce{Si}$、$\ce{Ge}$、$\ce{Ga}$、$\ce{As}$等),这些元素的导电性介于导体与绝缘体之间,可用于制造芯片、半导体器件。
2.寻找催化剂:过渡元素(副族和Ⅷ族元素)及其化合物常具有良好的催化性能,如铁用于合成氨工业、铂铑合金用于氨的催化氧化。
3.寻找耐高温、耐腐蚀材料:过渡元素中的钛($\ce{Ti}$)、钨($\ce{W}$)等,熔点高、硬度大、耐腐蚀,可用于制造航空航天材料、耐高温器械。
4.寻找农药原料:通常在第ⅤA、ⅥA、ⅦA族元素中寻找,如磷($\ce{P}$)、硫($\ce{S}$)、氯($\ce{Cl}$)等元素的化合物常具有杀菌、杀虫作用。
4.课堂小结与巩固(5分钟)梳理元素周期表的应用价值:预测元素性质、指导新材料研发、推动化学工业发展。课堂练习:布置作业:查阅资料,了解一种利用元素周期表研发的新材料及其应用场景,撰写简短报告。
1.下列元素中,最可能用于制造半导体材料的是( )
2.根据元素周期表,推测第6周期ⅡA族元素钡($\ce{Ba}$)的金属性与同主族钙($\ce{Ca}$)的金属性强弱关系,并说明理由。
微项目 海带提碘与海水提溴 —— 体验元素性质递变规律的实际应用
项目目标
1.通过海带提碘、海水提溴的实验探究与流程分析,体会元素周期律(卤素性质递变)在物质提取中的应用。
2.掌握物质分离提纯的基本方法(过滤、萃取、蒸馏),提升实验操作与流程设计能力。
3.认识海水资源的丰富性与利用价值,强化可持续发展意识和社会责任。
项目重难点
·重点:海带提碘的实验操作、海水提溴的流程设计与原理分析。
·难点:基于卤素性质递变规律选择合适的氧化剂、还原剂,优化提取流程。
项目准备
·实验用品:干海带、双氧水($\ce{H_{2}O_{2}}$溶液)、稀硫酸、淀粉溶液、四氯化碳($\ce{CCl_{4}}$)、海带灰、烧杯、漏斗、分液漏斗、试管、酒精灯、玻璃棒、铁架台。
·资料准备:海水提溴工业流程图、卤素单质氧化性强弱数据($\ce{Cl_{2}}$ > $\ce{Br_{2}}$ > $\ce{I_{2}}$)。
项目实施过程(1课时,45分钟)
1.项目导入与任务明确(5分钟)情境引入:展示海水资源分布图,介绍海水中含有的丰富元素(如氯、溴、碘等卤素元素),提问:“如何从海带、海水中提取具有重要应用价值的碘和溴?这一过程与卤素的性质递变有什么关系?”明确项目任务:
1.完成海带提碘的核心实验操作,验证碘的存在。
2.分析海水提溴的工业流程,解释各步骤的原理。
3.总结元素性质递变规律在物质提取中的应用。
2.任务一:海带提碘实验探究(20分钟)实验原理讲解:海带中含有碘离子($\ce{I^{-}}$),利用氧化剂(如$\ce{H_{2}O_{2}}$在酸性条件下)将$\ce{I^{-}}$氧化为碘单质($\ce{I_{2}}$),反应方程式:$\ce{2I^{-} + H_{2}O_{2} + 2H^{+} = I_{2} + 2H_{2}O}$;再利用碘单质易溶于有机溶剂(如$\ce{CCl_{4}}$)的性质,通过萃取分离碘。实验步骤(学生分组操作):小组讨论:
1.海带预处理:取少量干海带,用剪刀剪碎,放入烧杯中,加入适量蒸馏水,加热煮沸10分钟,使碘离子充分溶解;冷却后过滤,得到含$\ce{I^{-}}$的滤液。
2.氧化碘离子:向滤液中加入少量稀硫酸酸化,再逐滴加入双氧水,振荡,观察溶液颜色变化(溶液变为棕黄色,说明生成了$\ce{I_{2}}$)。
3.验证碘单质:取少量上述溶液,滴加2滴淀粉溶液,溶液变蓝,证明有碘单质存在。
4.萃取分离:将剩余溶液倒入分液漏斗中,加入适量四氯化碳,振荡后静置,观察分层现象(上层为无色水溶液,下层为紫红色碘的四氯化碳溶液)。
5.为什么选择双氧水作为氧化剂?能否用氯气替代?(双氧水氧化产物为水,无污染;氯气可替代,但过量氯气会进一步氧化$\ce{I_{2}}$,需控制用量,体现绿色化学思想)。
6.萃取时为什么选择四氯化碳?振荡分液漏斗时需要注意什么?(四氯化碳不溶于水、密度比水大,碘在其中溶解度远大于在水中;振荡时需及时放气,防止压强过大)。
任务二:海水提溴流程分析(15分钟)展示
可长按扫码下载完整电子版文档
▼ 
电脑端下载网址 https://jazpan.com/box/179.html
第 1 章 原子结构 元素周期律 第 1 节 原子结构与元素性质 第 2 节 元素周期律和元素周期表 第 3 节 元素周期表的应用 微项目 海带提碘与海水提溴 —— 体验元素性质递变规律的实际应用 本章自我评价 第 2 章 化学键 化学反应规律 第 1 节 化学键与物质构成 第 2 节 化学反应与能量转化 第 3 节 化学反应的快慢和限度 微项目 研究车用燃料及安全气囊 —— 利用化学反应解决实际问题 本章自我评价 第 3 章 简单的有机化合物 第 1 节 认识有机化合物 第 2 节 从化石燃料中获取有机化合物 第 3 节 饮食中的有机化合物 微项目 自制米酒 —— 领略我国传统酿造工艺的魅力 本章自我评价 附录 1. 各章节中的主要术语与物质名称 2. 本册教材中主要的实验内容 3. 常见元素中英文名称对照表 4. 部分酸、碱和盐的溶解性表(室温)
全册核心素养教案
·第 1 章 原子结构 元素周期律
o第 1 节 原子结构与元素性质
o第 2 节 元素周期律和元素周期表
o第 3 节 元素周期表的应用
o微项目 海带提碘与海水提溴 —— 体验元素性质递变规律的实际应用
o本章自我评价
鲁科版高中化学必修第二册第1章核心素养教案
一、本章课时安排
本章共设置8课时,具体分配如下:
·第1节 原子结构与元素性质:2课时
·第2节 元素周期律和元素周期表:2课时
·第3节 元素周期表的应用:2课时
·微项目 海带提碘与海水提溴:1课时
·本章自我评价:1课时
二、本章核心素养目标
1.宏观辨识与微观探析:能从宏观元素性质递变现象,探析原子结构(质子数、电子层数、最外层电子数)的微观本质,建立“结构决定性质”的认知模型。
2.证据推理与模型认知:通过分析实验数据、原子结构信息,推理元素周期律的本质;能运用元素周期表模型预测元素性质及化合物的化学性质。
3.科学探究与创新意识:参与元素性质递变、海带提碘等探究实验,体验科学探究的基本流程;能基于探究结果创新实验方案或优化物质提取流程。
4.科学态度与社会责任:认识元素周期律对化学研究、工业生产的指导价值;体会海水资源利用的意义,强化可持续发展意识和社会责任。
三、分节详细教案
第1节 原子结构与元素性质(第1课时:原子结构、核素与同位素)
教学目标
1.掌握原子的构成(原子核、质子、中子、电子)及各微粒间的数量关系。
2.理解质量数、核素、同位素的概念,能规范表示原子符号。
3.建立“原子结构决定元素种类、核素种类”的认知。
教学重难点
·重点:原子构成微粒的数量关系、核素与同位素的概念。
·难点:同位素的应用及元素相对原子质量的计算逻辑。
教学过程
1.情境导入(5分钟)展示卢瑟福α粒子散射实验示意图,提问:“实验中绝大多数α粒子穿过金箔,少数偏转,个别反弹,这一现象能说明原子的什么结构特点?”引导学生回顾初中原子结构知识,引出本节课核心问题:“原子的内部结构究竟是怎样的?各微粒之间有什么关系?”
2.新知探究一:原子的构成(15分钟)呈现电子、质子、中子的基本数据表(质量、相对质量、电量、电荷),组织学生小组讨论:学生汇报讨论结果,教师总结并板书核心关系式:即时练习:写出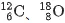 的质子数、中子数、核外电子数,巩固微粒数量关系。
的质子数、中子数、核外电子数,巩固微粒数量关系。
1.原子中质子数、核电荷数、核外电子数的关系及原因。
2.原子的质量主要由哪些微粒决定?
3.忽略电子质量时,原子相对质量与质子数、中子数的关系。
4.核电荷数 = 质子数 = 核外电子数
5.质量数(A)= 质子数(Z)+ 中子数(N)
6.原子符号表示:$\ce{_{Z}^{A}X}$(X为元素符号)
3.新知探究二:核素与同位素(15分钟)展示氕、氘、氚的原子结构示意图及相关信息(俗称、发现年份),提问:“这三种粒子的质子数、中子数、电子数有何异同?它们属于同一种元素吗?”引出核素概念:具有相同质子数和相同中子数的一类原子。进一步引导:“氕、氘、氚的质子数相同,中子数不同,它们之间是什么关系?”给出同位素定义:质子数相同而中子数不同的同一种元素的不同核素互为同位素。举例说明同位素的应用: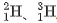 用于制造氢弹;
用于制造氢弹;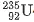 作为核反应堆燃料;放射性同位素用于示踪、探伤、医疗诊断等。补充元素相对原子质量的计算方法:各核素相对原子质量与丰度的乘积之和,结合氯元素两种核素
作为核反应堆燃料;放射性同位素用于示踪、探伤、医疗诊断等。补充元素相对原子质量的计算方法:各核素相对原子质量与丰度的乘积之和,结合氯元素两种核素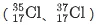 的丰度数据,演示计算过程。
的丰度数据,演示计算过程。
4.课堂小结与巩固(5分钟)梳理本节课核心知识点:原子构成→微粒关系→核素→同位素。课堂练习:判断下列说法是否正确:布置作业:查阅资料,了解一种放射性同位素的具体应用场景。
1.同种元素的不同核素化学性质完全相同(正确,质子数相同,最外层电子数相同)。
2.质子数相同的粒子一定是同种元素(错误,如$\ce{NH_{4}^{+}}$与$\ce{Na^{+}}$)。
第1节 原子结构与元素性质(第2课时:核外电子排布与元素性质)
教学目标
1.掌握核外电子分层排布的规律,能绘制核电荷数1-20号元素的原子结构示意图。
2.理解原子最外层电子数与元素得失电子能力、化合价的关系。
3.初步建立“电子排布决定元素化学性质”的认知模型。
教学重难点
·重点:核外电子排布规律、原子结构示意图的绘制。
·难点:原子结构与元素得失电子能力、化合价的关联。
教学过程
1.复习导入(5分钟)回顾上节课知识点:原子符号$\ce{_{Z}^{A}X}$的含义、同位素概念。提问:“同种元素的原子化学性质是否完全相同?为什么?”引出核外电子排布的重要性。
2.新知探究一:核外电子排布规律(15分钟)讲解核外电子分层排布的理论依据:能量低的电子离核近,能量高的电子离核远,电子层分为K、L、M、N、O、P、Q层(对应n=1-7)。呈现核外电子排布的核心规律:示范绘制钠原子($\ce{Na}$,核电荷数11)、氯原子($\ce{Cl}$,核电荷数17)的原子结构示意图,强调圆圈、弧线、数字的含义。学生分组练习:绘制核电荷数1-20号元素的原子结构示意图,小组内互相检查纠错,教师巡视指导。
1.各电子层最多容纳$2n^2$个电子(n为电子层数)。
2.最外层电子数不超过8个(K层为最外层时不超过2个)。
3.电子优先排布在能量较低的电子层,填满后再排布到能量较高的电子层。
3.新知探究二:原子结构与元素性质(15分钟)呈现稀有气体、金属、非金属元素的原子最外层电子数特点,组织学生讨论:总结规律:举例验证:钠原子(最外层1个电子)易失1个电子,呈+1价;氯原子(最外层7个电子)易得1个电子,呈-1价;氧原子(最外层6个电子)易得2个电子,呈-2价。拓展视野:介绍玻尔原子模型和电子云模型,说明核外电子运动的特殊性(无固定轨迹,仅能描述概率分布),加深学生对电子排布的理解。
1.稀有气体元素原子最外层电子数为8(氦为2),化学性质稳定,原因是什么?
2.金属元素原子最外层电子数一般小于4,非金属元素原子最外层电子数一般大于或等于4,这与它们的得失电子能力有何关系?
3.稀有气体元素:原子结构稳定,不易得失电子,化合价为0。
4.金属元素:易失去最外层电子形成阳离子,化合价为正价(数值等于失去的电子数)。
5.非金属元素:易得到电子形成阴离子,化合价为负价(数值等于得到的电子数)。
4.课堂小结与巩固(5分钟)梳理核心逻辑:电子分层排布→最外层电子数特点→元素得失电子能力→化合价。课堂练习:布置作业:结合原子结构示意图,分析第3周期元素原子得失电子能力的变化趋势。
1.下列原子结构示意图是否正确?若错误请改正:$\ce{Mg}$(+12 2 8 2)、$\ce{Si}$(+14 2 9 3)。
2.分析铝原子($\ce{Al}$)的最外层电子数,预测其得失电子能力及常见化合价。
第2节 元素周期律和元素周期表(第1课时:元素周期律)
教学目标
1.通过分析数据,探究原子序数递增时元素原子最外层电子数、原子半径、化合价的周期性变化。
2.理解元素周期律的含义及实质。
3.提升数据分析、归纳总结的科学探究能力。
教学重难点
·重点:元素周期律的具体表现(最外层电子数、原子半径、化合价的周期性变化)。
·难点:元素周期律的实质(原子核外电子排布的周期性变化)。
教学过程
1.情境导入(5分钟)展示元素周期表图片,提问:“目前已发现的110多种元素,为何能按照一定规律排列在周期表中?它们的性质之间存在怎样的内在联系?”引出本节课主题:元素性质随原子序数的递增是否存在规律性变化?
2.新知探究:元素周期律的探究(25分钟)呈现原子序数1-18号元素的相关数据(电子层数、最外层电子数、原子半径、常见化合价),组织学生进行分组探究:学生汇报探究结果,教师引导总结:引出元素周期律的定义:元素的性质随着元素原子序数的递增而呈周期性变化。深入分析实质:元素性质的周期性变化是原子核外电子排布周期性变化的必然结果(同周期元素电子层数相同,最外层电子数递增;同主族元素最外层电子数相同,电子层数递增)。拓展视野:介绍人类对元素周期律的认识历程(门捷列夫基于原子量的早期认识→莫斯莱基于核电荷数的修正→现代基于核外电子排布的本质认知),体现科学探究的渐进性。
1.以原子序数为横坐标,最外层电子数为纵坐标绘制柱状图,观察变化规律。
2.分析原子半径数据,总结同周期、同主族元素原子半径的变化趋势。
3.梳理各元素的常见化合价,找出化合价与最外层电子数的关系及变化规律。
4.最外层电子数:随原子序数递增,从1递增到8(第一周期除外),呈现周期性变化。
5.原子半径:同周期从左到右逐渐减小,同主族从上到下逐渐增大,呈现周期性变化。
6.化合价:正价从+1递增到+7(O、F除外),负价从-4递增到-1,呈现周期性变化。
3.课堂小结与巩固(10分钟)梳理探究流程:数据收集→图表分析→规律总结→揭示实质。课堂练习:布置作业:查阅资料,了解元素周期律在预测未知元素性质中的应用实例。
1.下列关于元素性质递变的说法错误的是( )
2.分析第2周期元素从$\ce{Li}$到$\ce{F}$的性质递变,说明其与核外电子排布的关系。
第2节 元素周期律和元素周期表(第2课时:元素周期表)
教学目标
1.掌握元素周期表的结构(周期、族的划分及特点)。
2.理解元素在周期表中的位置与原子结构的关系。
3.认识主族元素、副族元素、过渡元素、稀土元素的特点。
教学重难点
·重点:元素周期表的结构(周期、族的分类及数量)。
·难点:元素位置与原子结构(电子层数、最外层电子数)的关联。
教学过程
1.复习导入(5分钟)回顾元素周期律的核心内容及实质。提问:“元素周期律是通过什么载体直观呈现的?元素周期表的结构如何体现元素周期律?”引出本节课主题。
2.新知探究一:元素周期表的周期结构(10分钟)展示元素周期表,讲解周期的定义:元素周期表中的横行称为周期,周期序数等于该周期元素原子的电子层数。分析周期的分类及特点:强调:除第1周期外,每个周期都从最外层电子数为1的金属元素开始,过渡到最外层电子数为7的非金属元素,最后以最外层电子数为8的稀有气体元素结束。
1.短周期(1、2、3周期):分别含2、8、8种元素,电子层数依次为1、2、3。
2.长周期(4、5、6、7周期):分别含18、18、32、32种元素(第7周期为不完全周期,已发现所有元素),电子层数依次为4、5、6、7。
3.新知探究二:元素周期表的族结构(15分钟)讲解族的定义:元素周期表中的纵列称为族,共18个纵列,16个族。分类说明:举例说明:钠元素($\ce{Na}$)位于第3周期ⅠA族,电子层数3,最外层电子数1;氯元素($\ce{Cl}$)位于第3周期ⅦA族,电子层数3,最外层电子数7;碳元素($\ce{C}$)位于第2周期ⅣA族,电子层数2,最外层电子数4。拓展介绍:镧系元素(第6周期57-71号元素)、锕系元素(第7周期89-103号元素)的特点(原子结构相似、化学性质相近),及稀土元素的定义(ⅢB族钪、钇和镧系元素的统称)和应用价值。
1.主族(A族):由短周期和长周期元素组成,共7个主族(ⅠA-ⅦA),族序数等于最外层电子数。
2.副族(B族):仅由长周期元素组成,共7个副族(ⅠB-ⅦB)。
3.Ⅷ族:第8、9、10三个纵列,共1个族。
4.0族:第18纵列,由稀有气体元素组成,最外层电子数为8(氦为2),化学性质稳定。
4.新知探究三:元素周期表与原子结构的关系(5分钟)总结核心关联:学生练习:根据原子结构示意图判断元素在周期表中的位置,或根据元素位置推断原子结构。
1.周期序数 = 电子层数
2.主族序数 = 最外层电子数
3.原子序数 = 质子数 = 核电荷数 = 核外电子数
5.课堂小结与巩固(5分钟)梳理元素周期表结构:7个周期(3短4长)、16个族(7主7副1Ⅷ10)。课堂练习:布置作业:绘制元素周期表的结构示意图(标注周期、族的分类及数量)。
1.指出下列元素在周期表中的位置:$\ce{K}$(第4周期ⅠA族)、$\ce{Br}$(第4周期ⅦA族)、$\ce{Ar}$(第3周期0族)。
2.某元素位于第3周期ⅤA族,该元素的原子最外层电子数为______,电子层数为______,原子序数为______。
第3节 元素周期表的应用(第1课时:同周期、同主族元素性质递变)
教学目标
1.掌握同周期、同主族元素原子得失电子能力的递变规律。
2.学会通过实验或资料分析验证元素性质递变规律。
3.提升实验设计、证据推理的能力。
教学重难点
·重点:同周期(从左到右)、同主族(从上到下)元素得失电子能力的递变规律。
·难点:元素性质递变规律的实验验证与本质解释。
教学过程
1.复习导入(5分钟)回顾元素周期表的结构及原子结构与元素位置的关系。提问:“同周期、同主族元素的原子结构存在规律性变化,那么它们的化学性质(得失电子能力)会如何变化?如何验证这种变化?”
2.新知探究一:同周期元素性质递变(15分钟)明确研究对象:第3周期元素($\ce{Na}$、$\ce{Mg}$、$\ce{Al}$、$\ce{Si}$、$\ce{P}$、$\ce{S}$、$\ce{Cl}$)。提出问题:第3周期元素从左到右,原子失电子能力、得电子能力如何变化?实验探究(学生必做实验):比较钠、镁、铝的失电子能力。实验用品:金属钠(小块)、镁条、铝片、蒸馏水、酚酞溶液、烧杯、试管、镊子、砂纸。实验步骤:小组讨论:资料补充:展示$\ce{Si}$、$\ce{P}$、$\ce{S}$、$\ce{Cl}$与氢气反应的条件及氢化物稳定性数据:$\ce{SiH_{4}}$需高温下反应且不稳定,$\ce{PH_{3}}$加热易分解,$\ce{H_{2}S}$受热分解,$\ce{HCl}$稳定难分解。引导学生分析:同周期从左到右,非金属元素得电子能力逐渐增强(与氢气反应难度降低,氢化物稳定性增强)。
1.取3支试管,分别加入少量蒸馏水,滴加2滴酚酞溶液。
2.用镊子取一小块钠,吸干表面煤油后放入第一支试管,观察现象(钠浮在水面、剧烈反应、产生大量气泡、溶液变红),记录反应剧烈程度。
3.取一段镁条,用砂纸打磨去除氧化膜,放入第二支试管,观察现象(缓慢产生气泡,溶液微弱变红);加热试管,观察现象变化(反应加快,气泡增多,溶液红色加深)。
4.取一片铝片,用砂纸打磨去除氧化膜,放入第三支试管,观察现象(无明显气泡产生);加热试管,仍无明显气泡。
5.钠、镁、铝与水反应的剧烈程度排序:钠 > 镁(加热)> 铝(加热无明显现象),该现象说明三者失电子能力如何变化?(失电子能力:$\ce{Na}$ > $\ce{Mg}$ > $\ce{Al}$)
6.结合原子结构分析原因:同周期元素电子层数相同,从左到右质子数递增,原子核对最外层电子的吸引力增强,失电子能力逐渐减弱。
3.新知探究二:同主族元素性质递变(15分钟)明确研究对象:第ⅠA族($\ce{Li}$、$\ce{Na}$、$\ce{K}$)和第ⅦA族($\ce{F}$、$\ce{Cl}$、$\ce{Br}$、$\ce{I}$)元素。实验探究(演示实验):比较钠、钾的失电子能力。实验操作:分别取小块钠、钾,吸干煤油后放入盛有冷水的烧杯中,观察反应剧烈程度(钾与水反应比钠更剧烈,产生的氢气燃烧,并有轻微爆炸)。结论:第ⅠA族元素从上到下,失电子能力逐渐增强($\ce{Li}$ < $\ce{Na}$ < $\ce{K}$)。资料探究:分析第ⅦA族元素性质数据(单质氧化性、氢化物稳定性、置换反应):小组讨论:结合原子结构分析同主族元素性质递变原因:同主族元素最外层电子数相同,从上到下电子层数递增,原子核对最外层电子的吸引力减弱,失电子能力逐渐增强,得电子能力逐渐减弱。
1.氧化性:$\ce{F_{2}}$ > $\ce{Cl_{2}}$ > $\ce{Br_{2}}$ > $\ce{I_{2}}$(如$\ce{Cl_{2}}$能置换$\ce{NaBr}$溶液中的$\ce{Br_{2}}$,$\ce{Br_{2}}$能置换$\ce{KI}$溶液中的$\ce{I_{2}}$)。
2.氢化物稳定性:$\ce{HF}$ > $\ce{HCl}$ > $\ce{HBr}$ > $\ce{HI}$。
4.课堂小结与巩固(5分钟)总结递变规律:课堂练习:判断下列说法是否正确:布置作业:设计实验方案,验证第2周期元素$\ce{Li}$、$\ce{Be}$的失电子能力强弱。
1.同周期(左→右):失电子能力减弱,得电子能力增强;金属性减弱,非金属性增强。
2.同主族(上→下):失电子能力增强,得电子能力减弱;金属性增强,非金属性减弱。
3.第3周期元素从$\ce{Na}$到$\ce{Cl}$,金属性逐渐增强(错误)。
4.第ⅦA族元素从上到下,得电子能力逐渐减弱,氢化物稳定性逐渐降低(正确)。
第3节 元素周期表的应用(第2课时:元素周期表的实际应用)
教学目标
1.学会运用元素周期表预测未知元素的性质。
2.理解元素周期表在寻找新材料、指导化学研究等领域的应用价值。
3.强化“结构决定性质,性质决定用途”的化学观念。
教学重难点
·重点:元素周期表在预测元素性质、寻找新材料中的应用。
·难点:基于元素周期表的性质预测逻辑与应用。
教学过程
1.复习导入(5分钟)回顾同周期、同主族元素性质递变规律。提问:“掌握元素周期律和元素周期表的知识,能帮助我们解决哪些实际问题?科学家是如何利用元素周期表推动化学研究的?”引出本节课主题。
2.新知探究一:预测未知元素的性质(15分钟)案例分析:以第4周期ⅣA族元素锗($\ce{Ge}$)为例,预测其性质。引导学生思考:资料验证:展示锗的实际性质(半导体材料、$\ce{H_{2}GeO_{3}}$为弱酸、能与盐酸和强碱反应),验证预测的合理性。方法总结:预测未知元素性质的思路——先确定元素在周期表中的位置→找出相邻(同周期、同主族)已知元素→依据递变规律推测性质。学生练习:预测第5周期ⅥA族元素碲($\ce{Te}$)的最高价氧化物对应水化物的酸性强弱,及与氢气反应的难易程度。
1.锗在周期表中的位置:第4周期ⅣA族,相邻元素为硅($\ce{Si}$,上方)、锡($\ce{Sn}$,下方)、镓($\ce{Ga}$,左方)、砷($\ce{As}$,右方)。
2.依据同主族性质递变:硅是非金属,锡是金属,推测锗可能是半导体;硅的最高价氧化物对应水化物($\ce{H_{2}SiO_{3}}$)是弱酸,推测锗的最高价氧化物对应水化物($\ce{H_{2}GeO_{3}}$)也为弱酸,且酸性弱于$\ce{H_{2}SiO_{3}}$。
3.依据同周期性质递变:左方镓是金属,右方砷是非金属,进一步佐证锗的金属性弱于镓,非金属性弱于砷。
3.新知探究二:元素周期表在寻找新材料中的应用(15分钟)分类讲解应用场景:视频拓展:播放“元素周期表与新材料研发”短视频,展示周期表在新能源、新材料领域的最新应用,增强学生的直观认知。
1.寻找半导体材料:在金属与非金属的分界线附近(如$\ce{Si}$、$\ce{Ge}$、$\ce{Ga}$、$\ce{As}$等),这些元素的导电性介于导体与绝缘体之间,可用于制造芯片、半导体器件。
2.寻找催化剂:过渡元素(副族和Ⅷ族元素)及其化合物常具有良好的催化性能,如铁用于合成氨工业、铂铑合金用于氨的催化氧化。
3.寻找耐高温、耐腐蚀材料:过渡元素中的钛($\ce{Ti}$)、钨($\ce{W}$)等,熔点高、硬度大、耐腐蚀,可用于制造航空航天材料、耐高温器械。
4.寻找农药原料:通常在第ⅤA、ⅥA、ⅦA族元素中寻找,如磷($\ce{P}$)、硫($\ce{S}$)、氯($\ce{Cl}$)等元素的化合物常具有杀菌、杀虫作用。
4.课堂小结与巩固(5分钟)梳理元素周期表的应用价值:预测元素性质、指导新材料研发、推动化学工业发展。课堂练习:布置作业:查阅资料,了解一种利用元素周期表研发的新材料及其应用场景,撰写简短报告。
1.下列元素中,最可能用于制造半导体材料的是( )
2.根据元素周期表,推测第6周期ⅡA族元素钡($\ce{Ba}$)的金属性与同主族钙($\ce{Ca}$)的金属性强弱关系,并说明理由。
微项目 海带提碘与海水提溴 —— 体验元素性质递变规律的实际应用
项目目标
1.通过海带提碘、海水提溴的实验探究与流程分析,体会元素周期律(卤素性质递变)在物质提取中的应用。
2.掌握物质分离提纯的基本方法(过滤、萃取、蒸馏),提升实验操作与流程设计能力。
3.认识海水资源的丰富性与利用价值,强化可持续发展意识和社会责任。
项目重难点
·重点:海带提碘的实验操作、海水提溴的流程设计与原理分析。
·难点:基于卤素性质递变规律选择合适的氧化剂、还原剂,优化提取流程。
项目准备
·实验用品:干海带、双氧水($\ce{H_{2}O_{2}}$溶液)、稀硫酸、淀粉溶液、四氯化碳($\ce{CCl_{4}}$)、海带灰、烧杯、漏斗、分液漏斗、试管、酒精灯、玻璃棒、铁架台。
·资料准备:海水提溴工业流程图、卤素单质氧化性强弱数据($\ce{Cl_{2}}$ > $\ce{Br_{2}}$ > $\ce{I_{2}}$)。
项目实施过程(1课时,45分钟)
1.项目导入与任务明确(5分钟)情境引入:展示海水资源分布图,介绍海水中含有的丰富元素(如氯、溴、碘等卤素元素),提问:“如何从海带、海水中提取具有重要应用价值的碘和溴?这一过程与卤素的性质递变有什么关系?”明确项目任务:
1.完成海带提碘的核心实验操作,验证碘的存在。
2.分析海水提溴的工业流程,解释各步骤的原理。
3.总结元素性质递变规律在物质提取中的应用。
2.任务一:海带提碘实验探究(20分钟)实验原理讲解:海带中含有碘离子($\ce{I^{-}}$),利用氧化剂(如$\ce{H_{2}O_{2}}$在酸性条件下)将$\ce{I^{-}}$氧化为碘单质($\ce{I_{2}}$),反应方程式:$\ce{2I^{-} + H_{2}O_{2} + 2H^{+} = I_{2} + 2H_{2}O}$;再利用碘单质易溶于有机溶剂(如$\ce{CCl_{4}}$)的性质,通过萃取分离碘。实验步骤(学生分组操作):小组讨论:
1.海带预处理:取少量干海带,用剪刀剪碎,放入烧杯中,加入适量蒸馏水,加热煮沸10分钟,使碘离子充分溶解;冷却后过滤,得到含$\ce{I^{-}}$的滤液。
2.氧化碘离子:向滤液中加入少量稀硫酸酸化,再逐滴加入双氧水,振荡,观察溶液颜色变化(溶液变为棕黄色,说明生成了$\ce{I_{2}}$)。
3.验证碘单质:取少量上述溶液,滴加2滴淀粉溶液,溶液变蓝,证明有碘单质存在。
4.萃取分离:将剩余溶液倒入分液漏斗中,加入适量四氯化碳,振荡后静置,观察分层现象(上层为无色水溶液,下层为紫红色碘的四氯化碳溶液)。
5.为什么选择双氧水作为氧化剂?能否用氯气替代?(双氧水氧化产物为水,无污染;氯气可替代,但过量氯气会进一步氧化$\ce{I_{2}}$,需控制用量,体现绿色化学思想)。
6.萃取时为什么选择四氯化碳?振荡分液漏斗时需要注意什么?(四氯化碳不溶于水、密度比水大,碘在其中溶解度远大于在水中;振荡时需及时放气,防止压强过大)。
任务二:海水提溴流程分析(15分钟)展示
可长按扫码下载完整电子版文档

 点击阅读原文下载全册PPT课件电子版教案资料
点击阅读原文下载全册PPT课件电子版教案资料
