
 (期末复习讲义)
(期末复习讲义)
内容导航
明·期末考情:把握考试趋势方向,精准备考
理·核心要点:系统归纳知识脉络,构建体系
破·重难题型:攻克典型疑难问题,突破瓶颈
过·分层验收:阶梯式检测与评估,稳步提升

考查重点 | 命题角度 |
钠的性质及其应用 | 钠的物理性质;钠的化学性质;保存与用途的实际应用;钠的相关实验 |
钠的氧化物及其应用 | 物质类别与组成的判断;化学性质的对比与分析;性质与用途的对应关系;实验探究与现象分析;钠的氧化物相关计算 |
碳酸钠、碳酸氢钠的性质及其应用 | 物理性质的对比;化学性质的差异;相互转化关系;实验与鉴别、除杂;实际应用与综合计算 |
焰色试验及其应用 | 焰色试验的概念与原理的本质;焰色试验的实验操作的规范;焰色现象的判断与鉴别 |
钠及其化合物的转化 | 转化关系的基础判断;转化反应的离子方程式书写;转化关系的应用 |

 要点01 钠的性质及其应用
要点01 钠的性质及其应用
1.钠的物理性质
(1)颜色状态:色固体;
(2)硬度:很,可以用小刀切,剩余的钠要;
(3)密度:比水的,而比煤油的,比酒精的,即ρ煤油ρ钠ρ酒精ρ水。
(4)熔点:比较,原因:。
2.钠的化学性质
Na―――――――――――→O2、Cl2、H2O、H+等失去e-Na+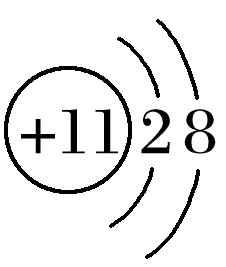
(1)与非金属单质(如O2、Cl2、S、H2)的反应
O2 | 常温 | 4Na+O2=2Na2O固体 |
加热 | 2Na+O2ΔNa2O2 固体 固体 |
Cl2 | 2Na+Cl2点燃2NaCl(产生火焰,生成) |
S | 2Na+S=Na2S(研磨时容易) |
H2 | 2Na+H2Δ2NaH(金属氢化物中,氢为价) |
(2)与水反应
①钠与水反应的产物:NaOH、H2
②与滴加酚酞的水反应的现象及解释
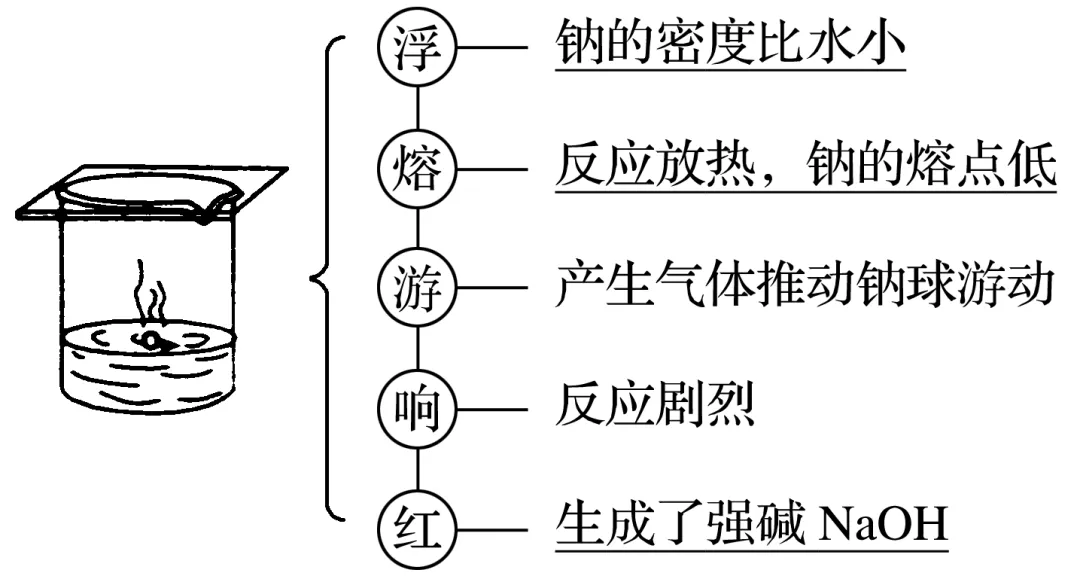
③实验结论:
化学方程式:、离子方程式:。
(3)与盐酸、硫酸反应
离子方程式:。
【易错提醒】Na先与反应,再与反应——先后。
(4)与盐反应
a.与熔融盐反应,如:、(制取金属钾,因为钾的沸点比钠的沸点低,使钾成为蒸汽而逸出)
b.与盐溶液反应
①投入NaCl溶液中,只有H2放出:
若投入饱和NaCl溶液中,有H2放出,还有晶体析出(温度不变)
②投入NH4Cl溶液中有H2和NH3逸出:
③投入CuSO4溶液中有H2逸出和蓝色沉淀生成:、
总反应:。
【易错提醒】与盐溶液反应时先与反应,生成的与盐可能发生反应。
3.钠的制取及保存
(1)工业制取:。
(2)保存:密封保存,通常保存在油或油中,钠易与空气中的反应,且钠的密度比煤油的密度,与煤油反应,故通常将少量钠保存在中,大量钠保存在中。
4.钠的用途
(1)钠钾合金(液态)可用于原子反应堆的剂。
(2)用作电光源,制作灯。
(3)冶炼某些金属:钠能与钛、锆、铌、钽等氯化物(熔融)发生置换反应,金属钠具有强还原性,熔融状态下可以用于制取金属,如。
(4)制取等化合物。
归|纳|总|结 |
1.钠燃烧时不能用水灭火,应用沙土盖灭。 2.取用金属钠时,用镊子夹取金属钠,用滤纸擦干表面的煤油,放在洁净干燥的玻璃片上用小刀切割,不能用手直接接触金属钠,并且将剩余的钠放回原试剂瓶中保存。 3.钠与溶液反应的共同现象 ①浮:钠浮在液面上;②熔:钠熔化成光亮的小球;③游:在液面上不停地游动直至反应完全;④响:反应中不停地发出“嘶嘶嘶”的响声。若溶液中H+浓度较大,与水相比反应更加剧烈,最后钠可能在液面上燃烧。 4.钠性质的巧记口诀:银白轻低软,传导热和电;遇氧产物变,遇氯生白烟;遇水记五点,浮熔游响红;遇酸酸优先,遇盐水在前。 5.考虑钠与酸、碱、盐的水溶液反应时,要注意Na与水反应的同时,生成的NaOH还可能继续与部分溶质反应。 6.对钠与酸反应的计算问题,勿忽略Na若过量还可与H2O反应。 |
 要点02 钠的氧化物及其应用
要点02 钠的氧化物及其应用
 1.氧化钠与过氧化钠的比较
1.氧化钠与过氧化钠的比较
| Na2O | Na2O2 |
电子式 | 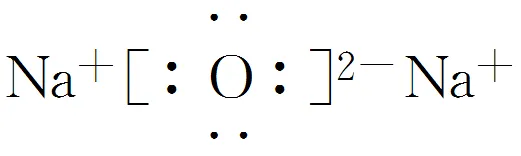
| 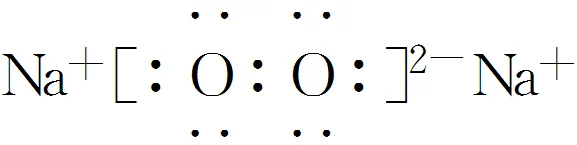
|
氧元素化合价 | | |
色、态 | 固体 | 色固体 |
阴、阳离子个数比 | 1∶2 | 1∶2 |
是否为碱性氧化物 | | |
化学键类型 | 只有键 | 有键和键 |
与水反应 | | |
与CO2反应 | | |
与盐酸反应 | | |
主要用途 | 可制烧碱 | 漂白剂、消毒剂、供氧剂 |
保存 | 密封 | 密封、远离易燃物 |
2.过氧化钠的性质:
(1)强氧化性的六个表现
试剂 | 现象 | 反应原理并解释 |
SO2气体 | - | |
FeCl2溶液 | | |
Na2SO3溶液 | - | |
氢硫酸 | | |
酚酞溶液 | | |
品红溶液 | | |
(2)理解Na2O2强氧化性的两个角度
①从结构角度
Na2O2的结构中含有过氧键(),含有过氧键结构的物质有的氧化性,以此类推,如H2O2、H2SO5(过硫酸,相当于H2O2中的一个H被—SO3H取代)、Na2S2O8(过二硫酸钠)中都有过氧键结构,都是很强的氧化剂。
②从化合价的角度
Na2O2中的氧元素为价,有很强的氧化性,能氧化一些常见的还原剂,如SO2、Fe2+、SO32-、HSO3-、H2S、S2-、I-。同时价的O也有还原性,如遇到强氧化剂KMnO4也可以被氧化成。
(3)Na2O2与H2O、CO2的反应规律
电子转移关系 | 当Na2O2与CO2、H2O反应时,物质的量关系为2Na2O2~O2~2e-,n(e-)=n(Na2O2)= |
气体体积变化关系 | 若CO2、水蒸气(或两混合气体)通过足量Na2O2,气体体积的减少量是原气体体积的12,等于生成氧气的量,ΔV=V(O2)= |
固体质量变化关系 | CO2、水蒸气分别与足量Na2O2反应时,固体相当于吸收了CO2中的“CO”、水蒸气中的“H2”,所以固体增加的质量Δm(CO2)=g·mol-1×n(CO2)、Δm(H2O)=g·mol-1×n(H2O) |
归|纳|总|结 |
①Na2O2遇KMnO4等强氧化剂时,表现出还原性,氧化产物为O2。 ②Na2O2遇H2O、H+则发生自身的氧化还原反应。 ③Na2O2遇还原性氧化物(即低价非金属氧化物),表现强氧化性,一般不生成氧气,而生成高价钠盐,如Na2O2+SO2===Na2SO4。 ④Na2O2遇最高价金属氧化物(酸酐)发生自身的氧化还原反应,有氧气生成,如2Mn2O7+2Na2O2===4NaMnO4+O2。 ⑤无论是过氧化钠还是其他过氧化物,具有强氧化性、漂白性等特殊性质的根本原因是这些物质中都含有过氧键。 |
 要点03碳酸钠、碳酸氢钠的性质及其应用
要点03碳酸钠、碳酸氢钠的性质及其应用
1、Na2CO3、NaHCO3的物理性质
2、Na2CO3、NaHCO3的化学性质
(1)热稳定性
①Na2CO3性质稳定,受热分解。
②NaHCO3性质不稳定,受热分解,化学方程式为。
(2)与足量盐酸反应
①Na2CO3:。
②NaHCO3:。
(3)与碱(NaOH溶液)反应
①Na2CO3:与NaOH溶液不反应。
②NaHCO3:。
(4)相互转化
①Na2CO3―→NaHCO3
向Na2CO3溶液中通入,化学方程式为。
②NaHCO3―→Na2CO3
NaHCO3固体加热分解转化成Na2CO3。
3、Na2CO3、NaHCO3的主要用途
(1)碳酸钠:用于造纸、制造、制皂、洗涤等。
(2)碳酸氢钠:用于制、医药、治疗过多、灭火剂等。
4、Na2CO3的制备—侯氏制碱法
①原料
食盐、氨气、二氧化碳——合成氨厂用水煤气制取氢气时的废气
其反应为,。
②反应原理
产生NaHCO3反应:。
产生Na2CO3的反应:。
③工艺流程
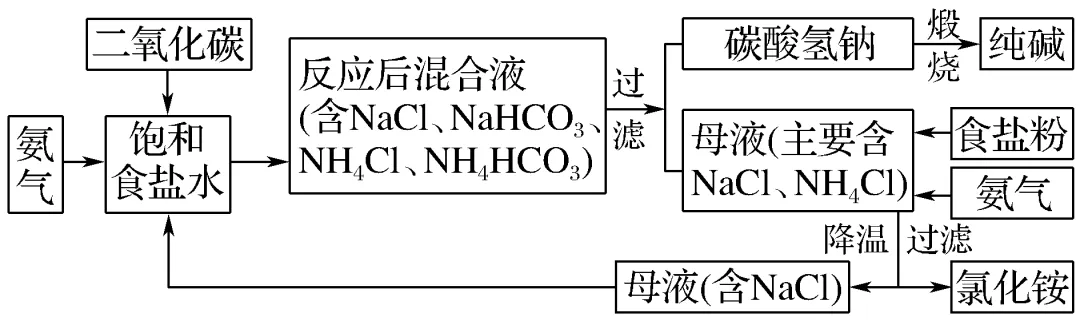
④循环使用的物质:、饱和食盐水。
5、Na2CO3、NaHCO3与盐酸反应的基本图象
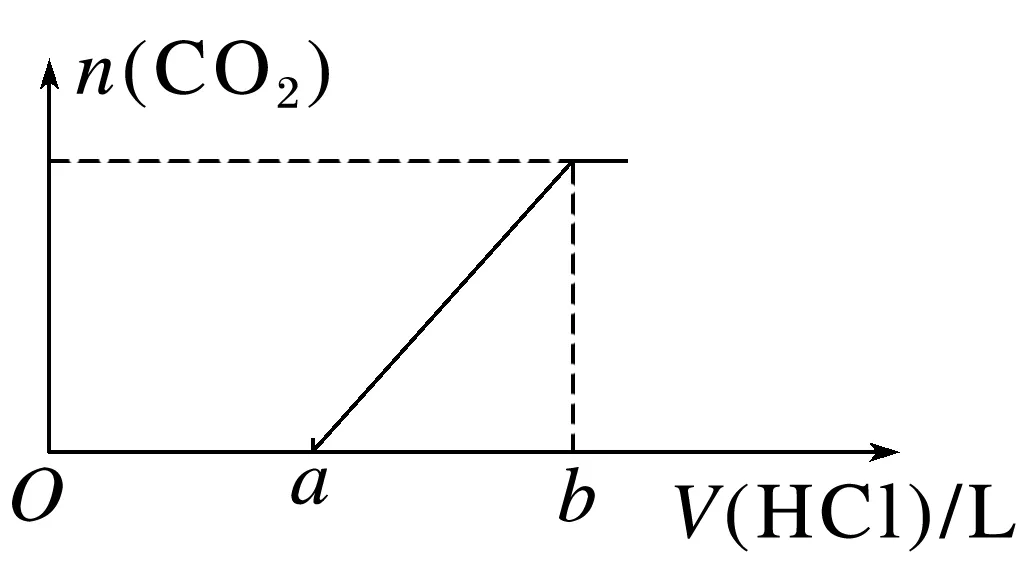
若V(Oa)=V(ab)(即Oa段与ab段消耗盐酸的体积相同) | 溶液中的溶质为 | 涉及离子方程式Oa:; ab: |
若V(Oa)>V(ab)(即Oa段消耗盐酸的体积大于ab段消耗盐酸的体积) | 溶液中的溶质为 | 涉及离子方程式Oa:、 ; ab: |
若V(Oa)<V(ab)(即Oa段消耗盐酸的体积小于ab段消耗盐酸的体积) | 溶液中的溶质为 | 涉及离子方程式Oa:; ab: |
若a=0(即图像从原点开始) | 溶液中的溶质为 | 涉及离子方程式: |
归|纳|总|结 |
1.Na2CO3、NaHCO3的鉴别 ①固体的鉴别用加热法:产生使澄清石灰水变浑浊的气体的是NaHCO3固体。 ②溶液的鉴别可用沉淀法、气体法和测pH法。 a.沉淀法:加入BaCl2溶液或CaCl2溶液,产生沉淀的是Na2CO3溶液。 b.气体法:滴入稀盐酸,立即产生气泡的是NaHCO3溶液。 c.测pH法:用pH试纸测相同浓度的稀溶液,pH大的是Na2CO3溶 2.Na2CO3、NaHCO3的除杂 序号 | 混合物(括号内为杂质) | 除杂方法 | ① | Na2CO3(s)(NaHCO3) | 加热法 | ② | NaHCO3(aq)(Na2CO3) | 通入足量CO2 | ③ | Na2CO3(aq)(NaHCO3) | 滴加适量NaOH溶液 |
3.易错提醒 ①NaHCO3与碱溶液反应的实质是HCO-3与OH-反应生成CO2-3,CO2-3有可能发生后续反应,如NaHCO3与Ca(OH)2溶液反应可以生成白色沉淀CaCO3; ②不能用澄清石灰水来鉴别Na2CO3与NaHCO3:Ca(OH)2溶液与二者反应均生成白色沉淀CaCO3,无法区别; ③用盐酸鉴别Na2CO3溶液和NaHCO3溶液时,要求两溶液浓度相差不大,且加入的盐酸等浓度且不宜过大;④Na2CO3、NaHCO3与酸、碱、盐的反应均为复分解反应,因而反应能否进行应从复分解反应的条件来判断。 |
 要点04焰色试验及其应用
要点04焰色试验及其应用
1.焰色试验的概念
很多金属或它们的化合物在灼烧时都会使火焰呈现特殊颜色,可以判断试样所含的金属元素,化学上把这样的称为焰色试验,属于物理变化,是元素的性质。
2.焰色试验的操作
铂丝――→酒精灯灼烧无色蘸取待测物――→酒精灯灼烧观察火焰颜色――→用盐酸洗涤铂丝――→酒精灯灼烧无色
3.常见元素的焰色
钠元素:色;钾元素:色(透过色钴玻璃观察);铜元素色;钡元素:色;钙元素:色。
归|纳|总|结 |
(1)焰色试验是物理变化,是金属元素的性质,既可以是单质,也可以是化合物,如不论灼烧Na2CO3、NaCl、Na2SO4还是钠的单质,均发出黄色火焰。 (2)用稀盐酸清洗的原因:生成金属氯化物,而金属氯化物在高温时可挥发,而硫酸盐难挥发。 (3)焰色反应中所用的火焰应是无色或浅色的。 (4)灼烧铂丝时应一直烧至火焰恢复到原来的颜色。 (5)可用洁净无锈的铁丝代替铂丝,不能用铜丝代替。 |
 要点05钠及其化合物的转化
要点05钠及其化合物的转化
1.钠及其重要化合物的知识主线:
Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3
2钠及其重要化合物知识网络
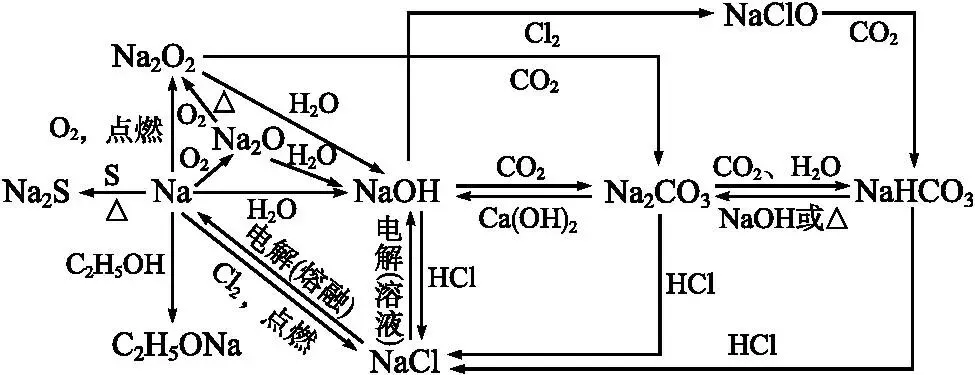 .
.
3.钠及其化合物的价类二维图
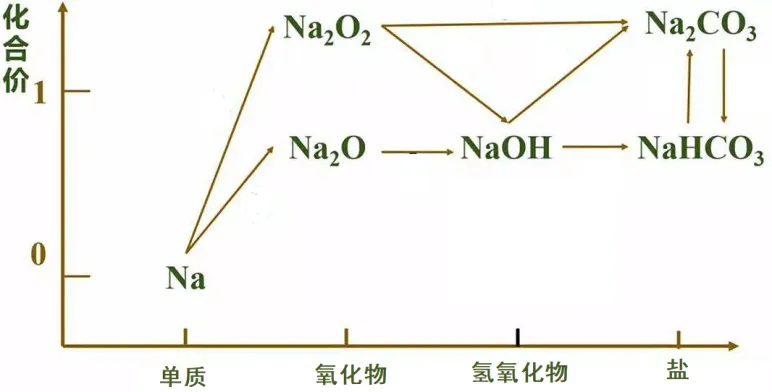
4.钠及其化合物重要方程式
①Na和H2O的反应:;
②Na在空气中燃烧:;
③Na2O2和H2O的反应:;
④Na2O2和CO2的反应:;
⑤向NaOH溶液中通入过量CO2:;
⑥将Na2CO3溶液与石灰乳混合:;
⑦向Na2CO3稀溶液中通入过量CO2:;
⑧将NaHCO3溶液和NaOH溶液等物质的量混合:;
⑨将NaHCO3溶液与澄清石灰水等物质的量混合:;
⑩将NaHCO3溶液与少量澄清石灰水混合:。
归|纳|总|结 |
钠及其化合物的知识盲点 (1)钠及其重要化合物: ①钠和盐溶液反应,不能置换出盐中的金属,与熔融的盐反应才可能置换出盐中的金属。 ②Na与足量O2反应无论生成Na2O还是Na2O2,只要参与反应的Na的质量相等,则转移电子的物质的量一定相等,但得到Na2O2的质量大于Na2O。 ③Na分别与H2O和乙醇发生反应均能生成H2,但反应的剧烈程度不同,前者反应剧烈,后者反应缓慢。 ④1 mol Na2O2参与反应转移电子的物质的量不一定为1 mol,如1 mol Na2O2与足量SO2的反应转移电子应为2 mol。 ⑤不能用Ca(OH)2溶液鉴别Na2CO3和NaHCO3溶液,应选用CaCl2或BaCl2溶液。 ⑥除去CO2中的HCl气体,应选用饱和的NaHCO3溶液。 ⑦向饱和的Na2CO3溶液中通入过量CO2,有NaHCO3 白色晶体析出。 ⑧焰色反应是元素的性质,无论游离态还是化合态,均具有相同的焰色反应,它不是化学变化,在观察钾元素的焰色反应时,应通过蓝色的钴玻璃片。 ⑨Na-K合金常温下呈液态,是原子反应堆的导热剂。 ⑩碱金属的密度呈现增大的趋势,但K反常。 ⑪Li和O2反应只生成Li2O;NaH是离子化合物,是一种强还原剂。Na2O、Na2O2阴阳离子个数比均为1∶2。 ⑫Na2O2投入品红溶液中,因溶液中有强氧化性物质,因而可使品红溶液褪色。Na2O2投入无色酚酞溶液中,酚酞溶液先变红后褪色。 |

 题型01 钠及其化合物的性质与用途
题型01 钠及其化合物的性质与用途
【典例1】(25-26高一上·安徽六安·期中)下列有关钠及其化合物的说法正确的是
A.实验室钠着火时,可以用二氧化碳灭火器灭火
B.钠比铁活泼,可以利用钠将溶液中的铁置换出来
C.向和固体中加入少量水均会放出热量
D.中学实验室中可将未用完的钠放回原试剂瓶
【变式1-1】(25-26高一上·广东广州·期中)下列关于钠及其化合物的叙述正确的是
A.金属钠保存在煤油里,说明金属钠的密度比煤油的小
B.金属钠与水反应时会熔化,说明钠的熔点低且反应放热
C.分别加热和固体,试管内壁均有水珠,说明两种物质均受热分解
D.盐酸分别滴加到同浓度的碳酸钠和碳酸氢钠,溶液中放出气体的速度:>
【变式1-2】(24-25高一上·福建宁德·期末)关于钠及其化合物的说法错误的是
A.金属钠是一种银白色金属,可保存在煤油中
B.氧化钠和过氧化钠均可与盐酸反应,产物完全相同
C.氢氧化钠俗称烧碱,具有较强的腐蚀性
D.Na2CO3溶液和NaHCO3溶液都能与Ca(OH)2溶液反应得到白色沉淀
 题型02 钠及其化合物的转化关系
题型02 钠及其化合物的转化关系
【典例2】(25-26高一上·广东茂名·期中)以不同类別物质间的转化为线索,认识钠及其化合物。下列分析正确的是
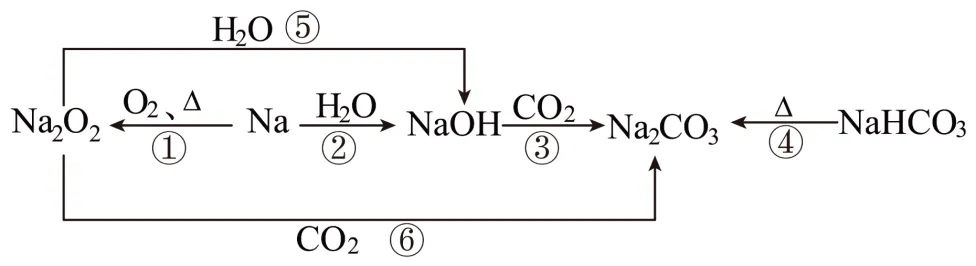
A.上述转化中含有分解反应和置换反应
B.在水溶液中电离方程式为:
C.反应③④表明不能转化为NaOH或
D.反应⑤中只做氧化剂
【变式2-1】(24-25高一上·广东广州·期末)下图为钠元素的价类二维图。下列有关叙述不正确的是
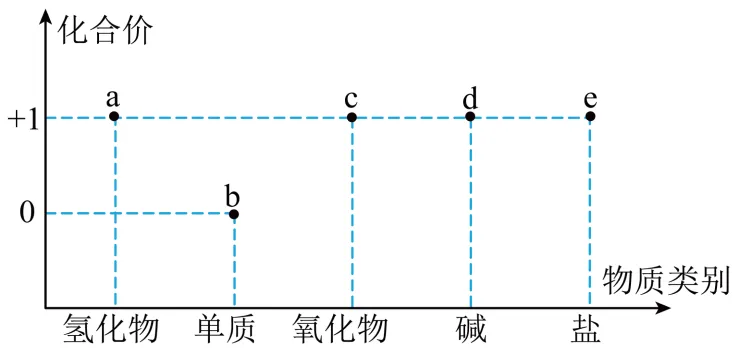
A.若a是NaH,其中氢元素的化合价为-1价
B.b能与水剧烈反应产生氢气
C.若c为Na2O2,可用作潜水艇的供氧剂
D.若e是Na2CO3,向其溶液中逐滴滴加盐酸可立即产生气泡
【变式2-2】(24-25高一上·云南·期末)下图中,A是单质,B为淡黄色物质,A、B、C、D和E均含同一种元素。下列叙述错误的是
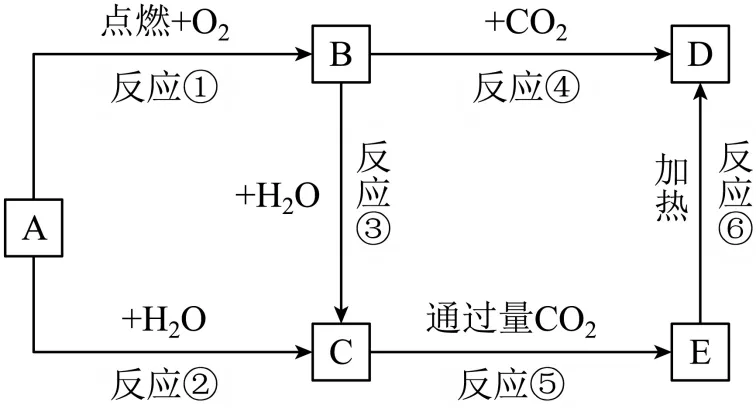
A.热稳定性:E>D
B.物质B的电子式是
C.常温下,物质D在水中的溶解度大于E在水中的溶解度
D.反应③中,当生成0.2molC时,转移的电子的物质的量为0.1mol
 题型03 钠及其化合物的制备与性质探究
题型03 钠及其化合物的制备与性质探究
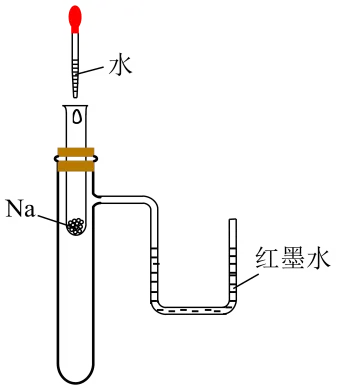
【典例3】(24-25高一上·河北保定·期末)下列实验装置能达到实验目的的是:
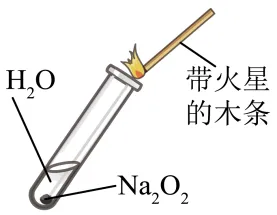
①验证 Na 和水反应是否为放热反应 | ②检验Na2O2与H2O反应有O2生成 |
| 
|
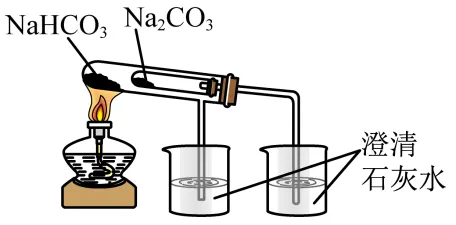
③观察 K2CO3的焰色试验 | ④比较、的稳定性 |
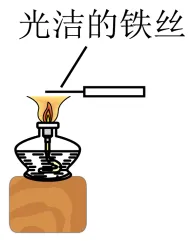
| 
|
A.①②B.①③C.②③D.③④
【变式3-1】(24-25高一上·河南·期末)某实验小组通过如图所示实验,探究与水的反应。下列说法错误的是
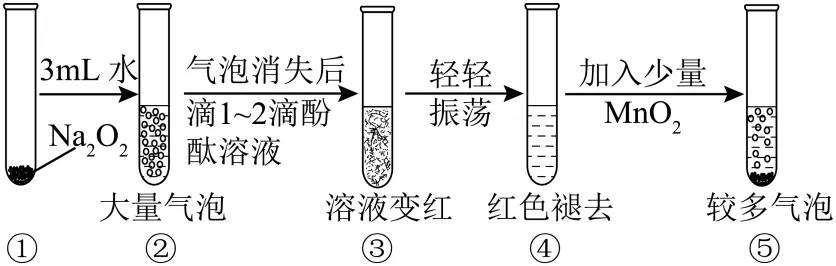
A.③中溶液变红,说明有碱性物质生成
B.④中现象可能是溶液中含有强氧化性物质造成的
C.⑤中的主要作用是验证溶液中存在
D.②中的大量气泡主要成分是氢气
【变式3-2】(24-25高一上·北京丰台·期末)钠与水反应的微型实验装置如图所示。下列说法不正确的是
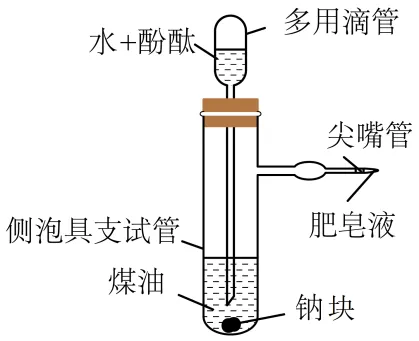
A.肥皂液可用于收集反应产生的B.反应时,钠块熔为小球,说明钠的硬度小
C.钠块在煤油和水交界处上下跳动,直至消失D.反应后试管中液体分层,下层呈红色
 题型04 侯氏制碱法工艺流程
题型04 侯氏制碱法工艺流程
【典例4】(24-25高一上·北京西城·期末)侯氏制碱法工艺流程如图所示。
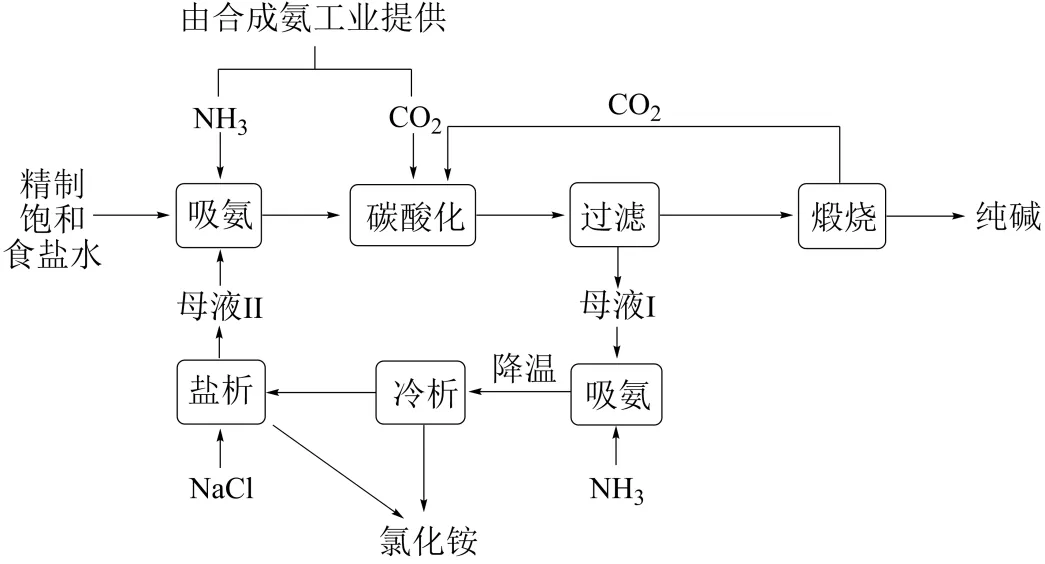
下列说法不正确的是
A.饱和食盐水“吸氨”的目的是使“碳酸化”时产生更多的
B.煅烧时发生反应
C.“盐析”后溶液比“盐析”前溶液大
D.母液II与母液I所含粒子种类相同,但前者、、的浓度更大
【变式4-1】(24-25高一上·江苏苏州·期末)实验室用下图装置模拟侯氏制碱法原理,以NaCl、、等为原料制取少量。下列有关说法正确的是
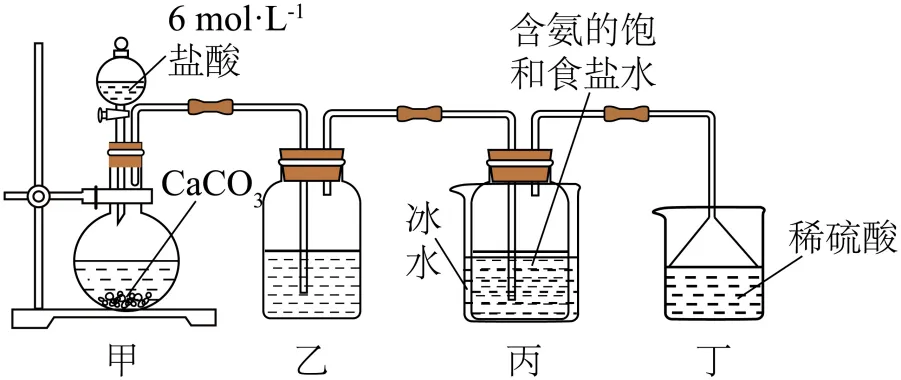
A.除去中的少量HCl可在乙装置中加入饱和溶液
B.用冰水浴冷却丙装置有利于析出固体
C.丙装置中析出固体的上层清液中不存在
D.丁装置是为了吸收丙装置中逸出的和
【变式4-2】(25-26高一上·安徽·开学考试)某制碱工厂以粗盐为原料制纯碱,部分工艺流程如图:

有关说法正确的是
A.流程中加入三种溶液的顺序不能调整
B.按流程所加溶液的顺序除杂,过滤后得到三种沉淀
C.流程通入氨气之后溶液呈碱性,促进吸收
D.流程中发生反应的化学方程式为
 题型05 焰色试验
题型05 焰色试验
【典例5】(25-26高一上·甘肃张掖·期中)春节期间,兰州太平鼓舞、永登硬狮子舞、何家营滚灯等非遗项目纷纷亮相,除此之外还有五颜六色的烟花秀,这与高中化学中“焰色试验”知识相关,下列说法中正确的是
A.钠燃烧时发出黄色的火焰
B.焰色试验中发生的变化为化学变化
C.透过蓝色钴玻璃观察到焰色为紫色,则待测液一定为钾盐
D.可用稀硫酸代替稀盐酸洗涤焰色试验中用到的铂丝
【变式5-1】(25-26高一上·黑龙江牡丹江·期中)焰色试验中钾盐在灼烧时火焰呈
A.黄色B.紫色C.绿色D.砖红色
【变式5-2】(25-26高一上·山东临沂·期中)五彩缤纷的焰火与“焰色试验”知识有关。下列有关“焰色试验”的说法正确的是
A.焰色试验前,应用稀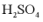 清洗铂丝
清洗铂丝
B.Na、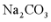 、
、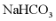 灼烧时火焰颜色均为黄色
灼烧时火焰颜色均为黄色
C.将KCl在酒精灯上灼烧时能直接观察到紫色火焰
D.焰色试验是元素的性质,属于化学变化
 题型06 钠及其化合物的相关计算
题型06 钠及其化合物的相关计算
【典例6】(25-26高一上·新疆乌鲁木齐·期中)46 g乙酸在足量氧气中完全燃烧后的产物全部通入足量的过氧化钠中,充分反应后,固体增加的质量为
A.48 gB.16 gC.46 gD.80 g
【变式6-1】(24-25高一上·河南·期末)实验室中,将17g在空气中部分变质的粉末样品溶于20mL水中,收集到2.4g气体,然后向水溶液中加入200g质量分数为7.3%的盐酸恰好完全反应,则m(发生变质的)(未变质的)为
A.1∶1B.1∶3C.3∶1D.无法确定
【变式6-2】(24-25高一上·浙江台州·期末)某小组对加热了的固体进行探究,取该样品溶于水制成溶液,向此溶液中缓慢滴加一定浓度的盐酸,并不断搅拌。随着盐酸的加入溶液中有关离子的物质的量的变化如图所示。则下列有关说法正确的是
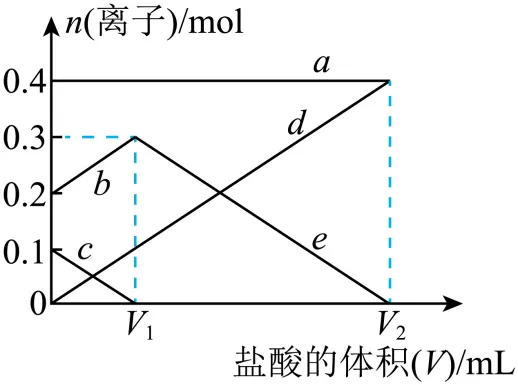
A.a、d、e曲线对应的离子分别是、、
B.样品溶液中
C.加热前的总质量为33.6g
D.消耗盐酸的体积


期末基础通关练(测试时间:10分钟)
 1.(25-26高一上·青海海南·期中)下列关于钠的叙述中错误的是
1.(25-26高一上·青海海南·期中)下列关于钠的叙述中错误的是
A.钠原子的最外电子层上只有1个电子B.钠燃烧时生成氧化钠
C.钠具有很强的还原性D.钠燃烧时发出黄色的火焰
2.(25-26高一上·河北衡水·期中)联合制碱法为我国的化学工业发展和技术创新做出了重要贡献。发明联合制碱法的化学家是
A.屠呦呦B.门捷列夫C.徐光宪D.侯德榜
3.(25-26高一上·浙江宁波·期中)节日燃放的烟花利用了“焰色试验”的原理,下列说法正确的是
A.焰色试验属于化学变化
B.铂丝应用稀硫酸清洗后在火焰上灼烧至与原火焰颜色相同,再蘸取样品实验
C.若火焰呈黄色,则该样品中仅含有钠元素
D.实验时,应尽可能使用火焰颜色较浅的煤气灯
4.(25-26高一上·北京·期中)关于和性质的有关叙述正确的是
A.在水中的溶解性:
B.热稳定性;
C.与酸反应的速度:
D.和在一定条件下可以相互转化
5.(25-26高一上·浙江·期中)将一块金属钠投入足量的下列溶液中,既能生成气体,又能生成白色沉淀的是
A.稀硫酸B.稀溶液C.溶液D.溶液
6.(25-26高一上·黑龙江牡丹江·月考)下列关于氧化钠和过氧化钠的叙述正确的是
A.在与水的反应中,既是氧化剂又是还原剂
B.和都是白色固体,都能与冷水作用得到和
C.一个氧化钠和一个过氧化钠中的阴离子个数比为
D.与都能与水反应生成碱,它们都是碱性氧化物
7.(24-25高一上·广西来宾·期中)钠的化合物有多种用途:
Ⅰ.过氧化钠是重要的化工原料,具有多种用途。
(1)过氧化钠是色固体。
(2)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出Na2O2和CO2反应的化学方程式:。
(3)过氧化钠可与水反应,写出Na2O2和H2O反应的化学方程式:。
Ⅱ.
(4)NaHCO3俗称小苏打,在制做糕点时添加,在受热时产生气体,请写出相关的化学反应方程式:;它还可以用于治疗胃酸过多,请写出相关的化学反应方程式:。
 (测试时间:10分钟)
(测试时间:10分钟)
 1.(25-26高一上·陕西商洛·期中)以不同类别物质间的转化为线索,可结构化地认识钠及其化合物的性质。下列说法不正确的是
1.(25-26高一上·陕西商洛·期中)以不同类别物质间的转化为线索,可结构化地认识钠及其化合物的性质。下列说法不正确的是
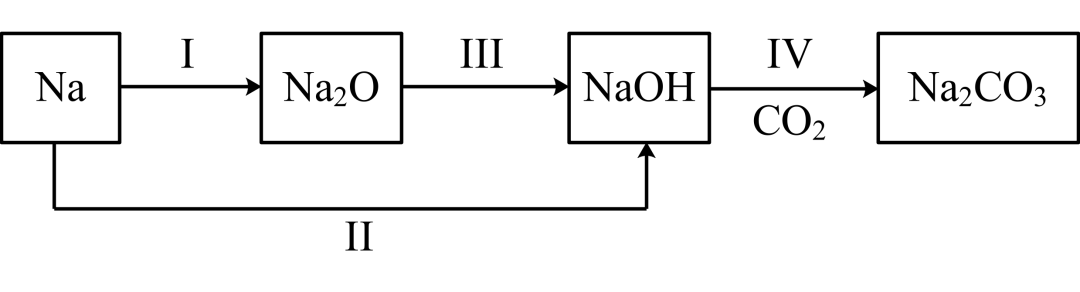
A.过程Ⅱ发生反应的离子方程式为
B.若改变过程I的反应条件,能得到淡黄色固体
C.钠常保存于煤油中,钠着火时,应使用专用灭火剂或干砂灭火
D.上述过程I~IV中,发生电子转移的是I、II
2.(25-26高一上·甘肃张掖·期中)下列说法错误的是
A.可用澄清的石灰水鉴别和两种溶液
B.溶液和盐酸可以通过互滴进行鉴别
C.向碳酸钠固体中加入少量水后,结块变成晶体
D.向碳酸钠溶液中滴入酚酞,溶液变为红色
3.(25-26高一上·广东广州·期中)下表中,对陈述I、Ⅱ的正确性及二者间是否具有因果关系的判断都正确的是
选项 | 陈述I | 陈述Ⅱ | 判断 |
A | Na可与水反应产生 | Na着火不能用水扑灭 | I对;Ⅱ对;有关系 |
B | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | I对;Ⅱ对;有关系 |
C | 过氧化钠可用作航天员供氧剂 | 
| I对;Ⅱ对;有关系 |
D | 小苏打可用于治疗胃酸过多 | 
| I对;Ⅱ对;有关系 |
4.(25-26高一上·山西太原·月考)“价-类”二维图是学习元素化合物知识的重要模型和工具,图1为钠的“价-类”二维图,图2为比较甲、乙(甲、乙为Na2CO3或NaHCO3)的热稳定性的实验装置。下列说法正确的是
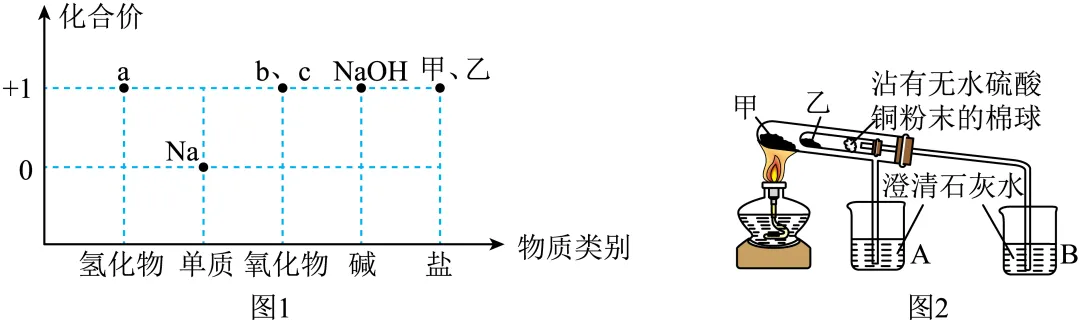
A.a与水生成NaOH的反应中氧化产物与还原产物的质量之比为
B.相同个数的b和c,含有的离子总数不同
C.Na转化为b或c,主要取决于反应温度和O2的量
D.甲为NaHCO3,可用于治疗胃酸过多
5.(25-26高一上·北京·期中)下列关于和的说法不正确的是
A.和的水溶液均可使酚酞溶液变红
B.比稳定
C.可用溶液将转化为
D.可用加热的方法鉴别和
6.(25-26高一上·新疆乌鲁木齐·期中)有关钠及其化合物,下列叙述正确的是
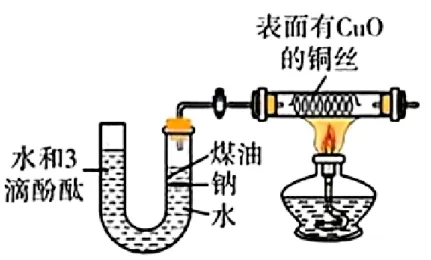
A.金属钠着火,可用水或灭火器扑灭
B.金属钠投入坩埚中加热,出现白色固体
C.金属钠投入溶液中,有红色金属铜析出
D.金属钠投入右侧U形管中,其可能在煤油和水交界处上下跳动,直至消失
7.(25-26高一上·黑龙江哈尔滨·期中)回答下列问题:
(1)钠有一种常见淡黄色氧化物,名称为,常用作呼吸面具的供氧剂。该物质与反应的化学反应方程式为。
(2)1 mol钠单质中含有钠原子约为个,含有质子mol,在与足量的水反应中失去mol电子。
(3)金属钠放置在空气中观察到下列现象。
银白色固体变灰暗变白色出现液滴白色晶体
①反应I后固体变灰暗,该固体的化学式为,将少量灰暗色固体投入溶液中,观察到的实验现象为。
②反应Ⅱ后得到的固体为,在水中的电离方程式为。
③反应Ⅳ,主要是液滴与空气中的(填名称)发生反应,下列属于白色晶体用途的是(填字母)。
A.制肥皂B.造纸
C.烘焙蛋糕D.用于治疗胃酸过多症
 (测试时间:15分钟)
(测试时间:15分钟)
 1.(25-26高一上·江西·期中)将2.3 g Na加入100 g溶质质量分数为16%的溶液中。充分反应后,下列说法正确的是
1.(25-26高一上·江西·期中)将2.3 g Na加入100 g溶质质量分数为16%的溶液中。充分反应后,下列说法正确的是
A.可生成0.05 mol CuB.可生成0.1 mol
C.反应后的溶液总质量为102.3 gD.反应后的溶液中,的质量为8 g
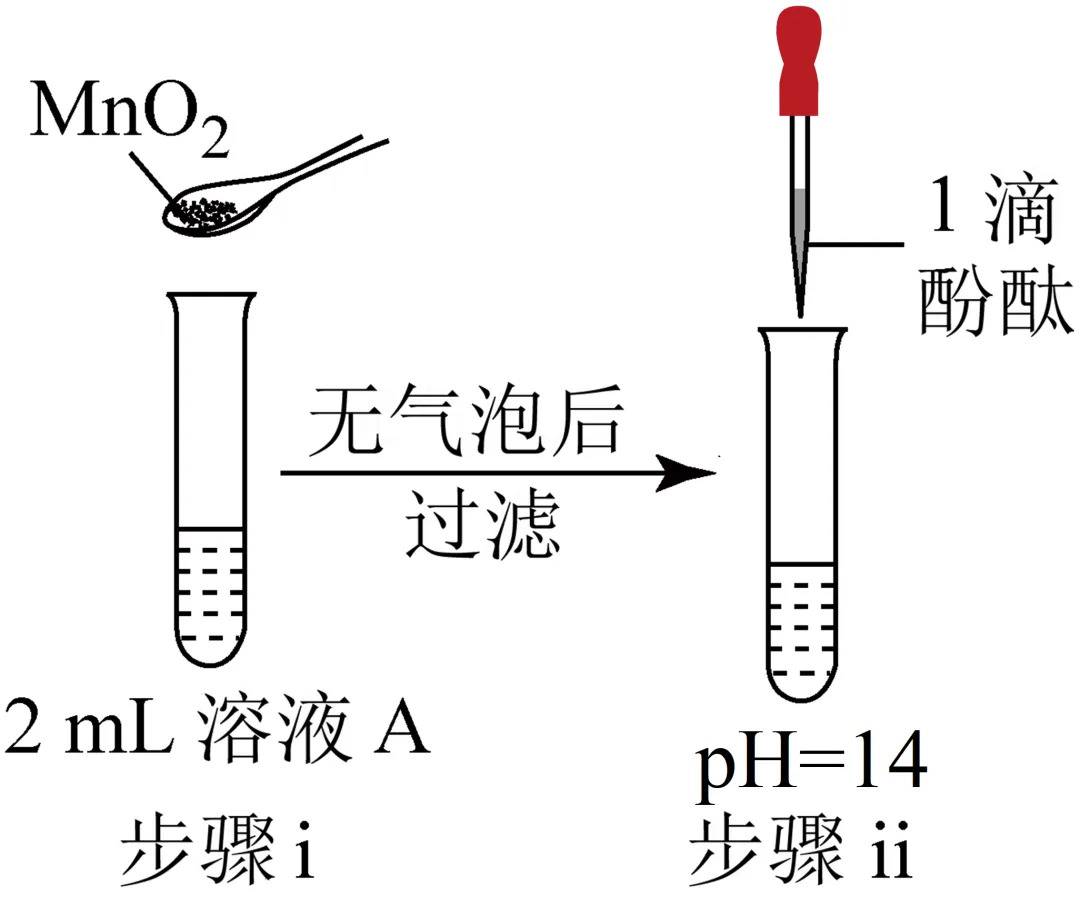
2.(25-26高一上·北京·期中)研究小组探究与水反应。取1.56 g 粉末加入到40 mL水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验。
编号 | ① | ② | ③ | ④ |
操作 | 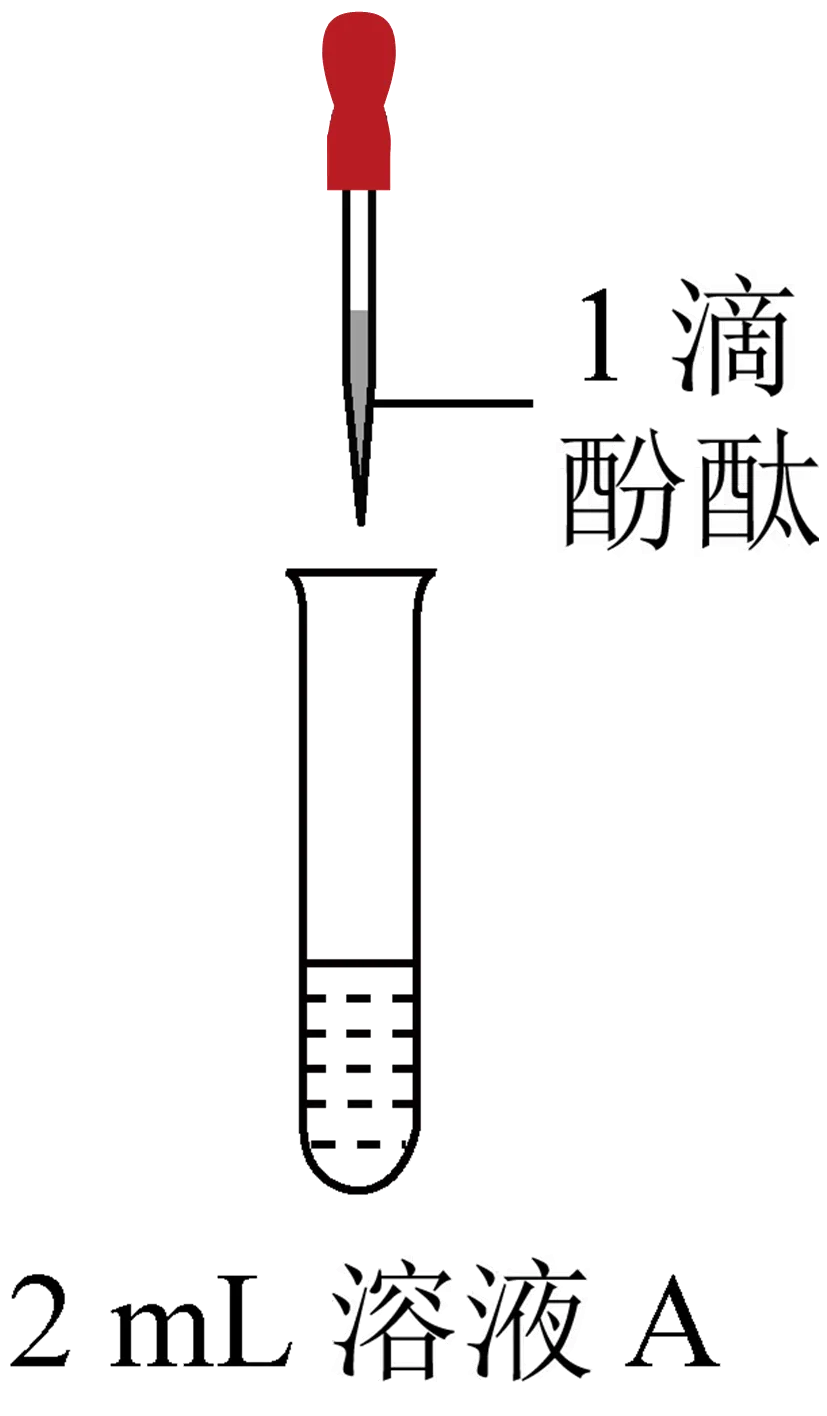
| 
| 
| 
|
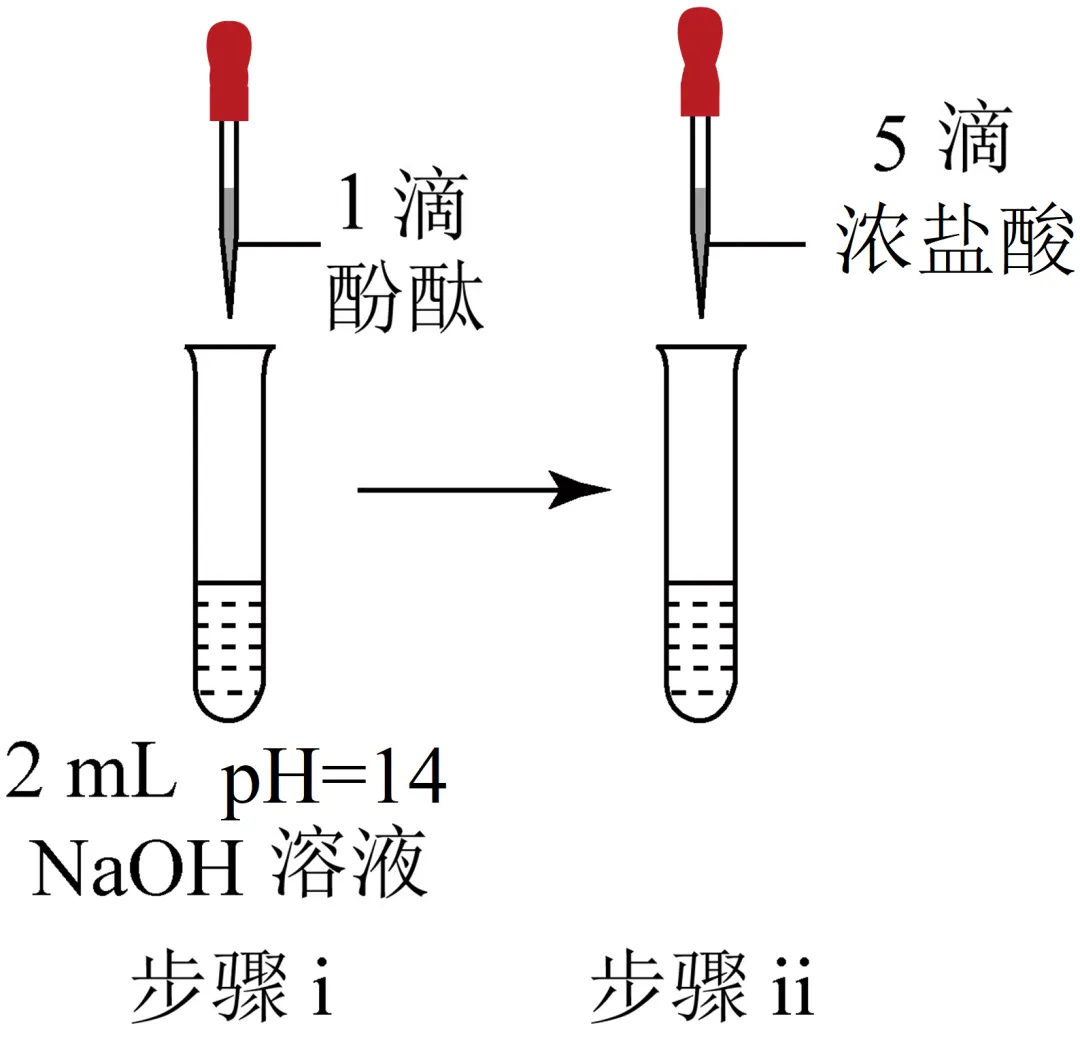
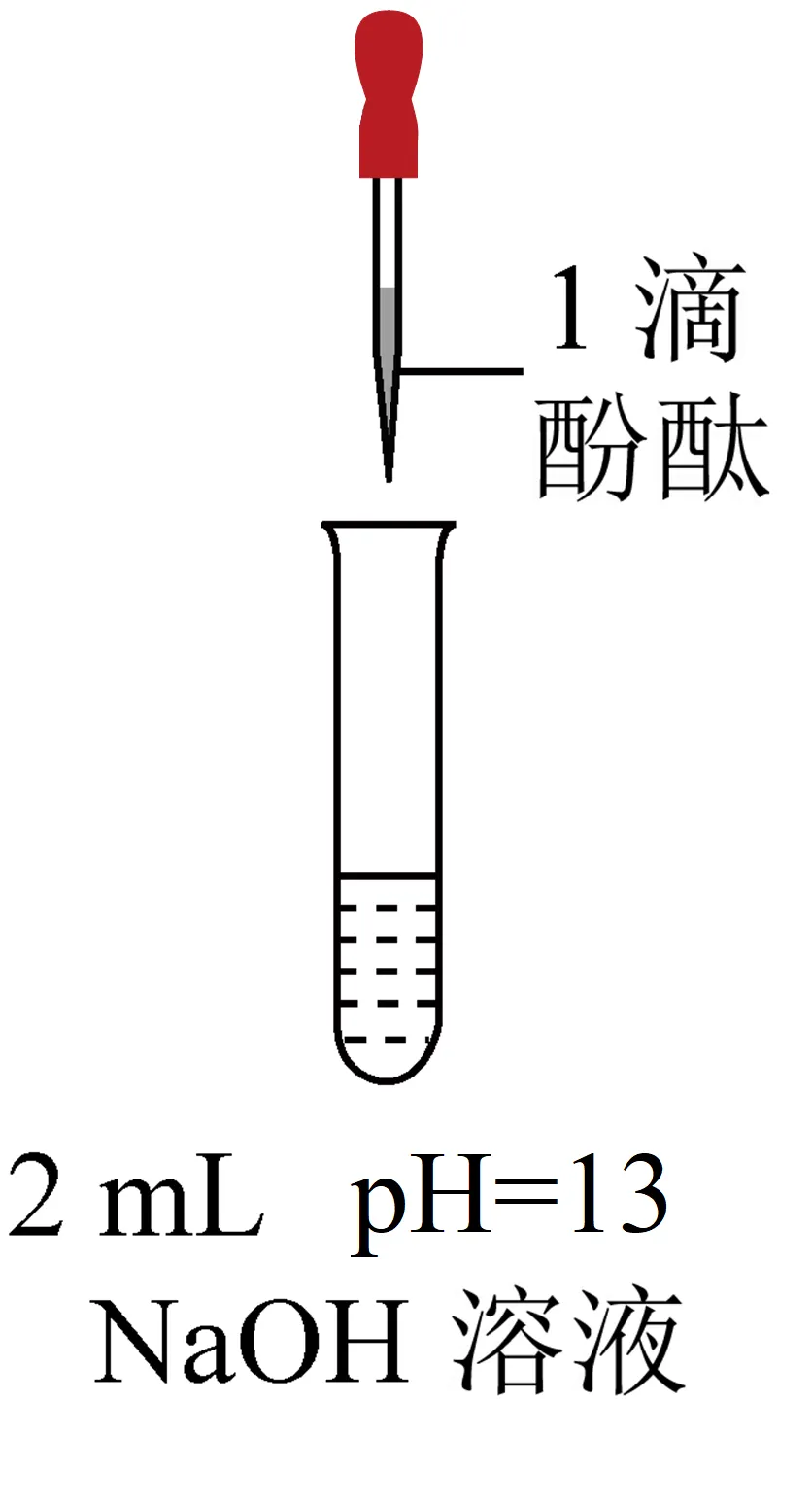
现象 | 溶液变红色,20秒后褪色 | ⅰ.产生大量能使带火星木条复燃的气体 ⅱ.溶液变红色,10分钟后褪色 | ⅰ.溶液变红色,10分钟后溶液褪色 ⅱ.变红色 | 溶液变红色,2小时后无明显变化 |
下列说法不正确的是
A.由②中现象ⅰ可知,与水反应有生成
B.由③、④可知,②中溶液红色褪去是因为浓度大
C.由②、③、④可知,①中溶液红色褪去的主要原因不是浓度大
D.向①中褪色后的溶液中滴加5滴浓盐酸,溶液最终变成红色
3.(25-26高一上·甘肃张掖·期中)下列关于钠及其化合物的叙述中正确的说法有
①钠的2种氧化物中阴、阳离子个数比均为1:2
②新切开的钠的光亮的表面很快变暗是因为生成了
③可用水来确定某粉末中是否含有
④钠着火后不能用水扑灭,可用泡沫灭火器或沙土来灭火
⑤钠可以把铜、铁等金属从它们的化合物的水溶液中置换出来
A.3个B.4个C.1个D.2个
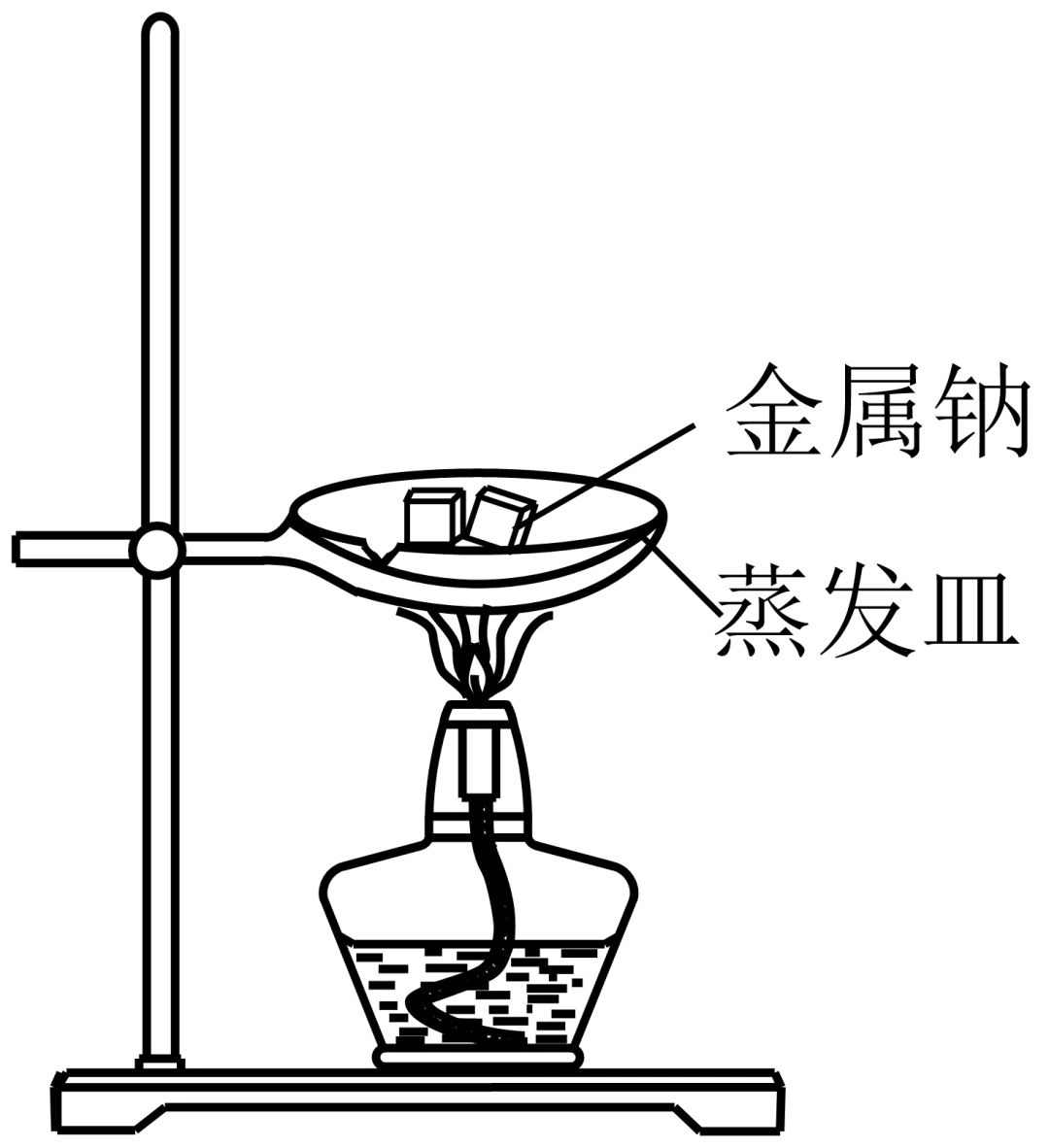
4.(25-26高一上·黑龙江哈尔滨·期中)如图所示,在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水硫酸铜粉末与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成。据此判断下列说法错误的是
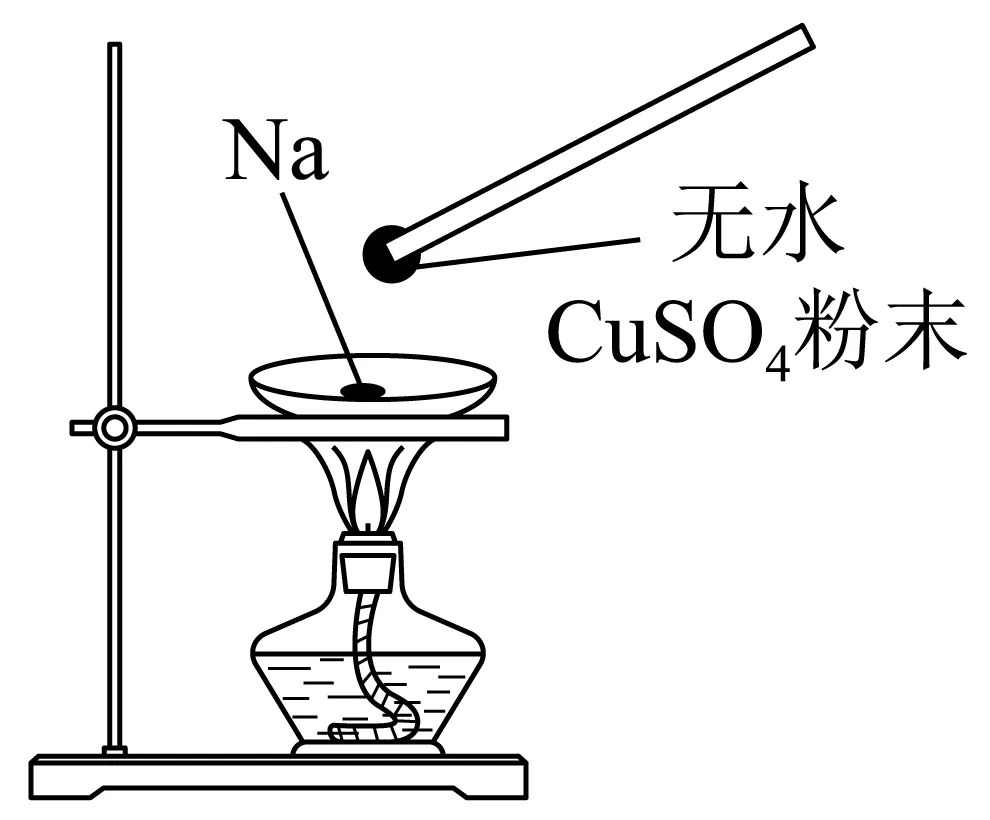
A.上述反应的化学方程式为
B.上述反应中钠表现了还原性
C.上述反应中若有1 mol钠参与反应,则转移1 mol电子
D.若将钠投入硫酸铜稀溶液中,也有铜单质被钠置换生成
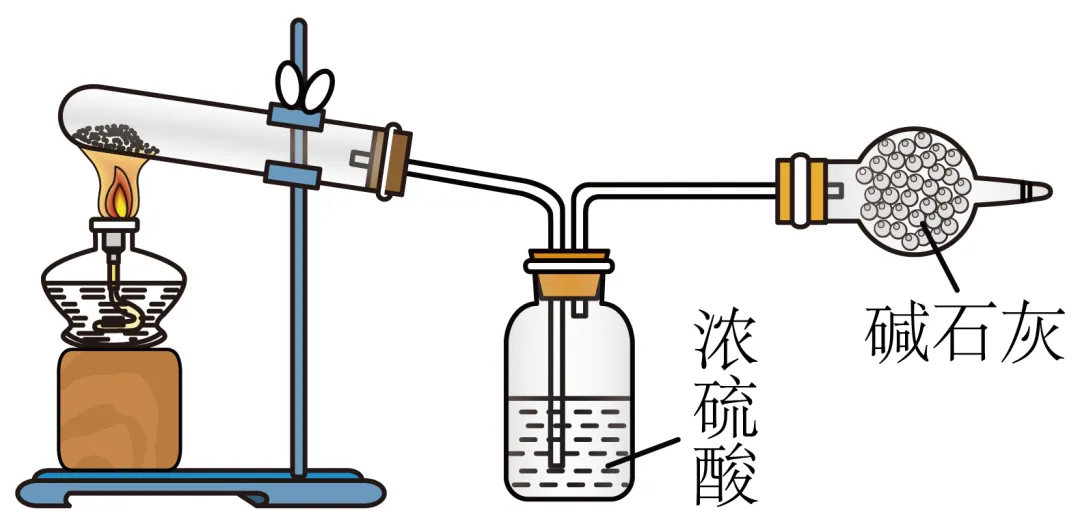
5.(25-26高一上·黑龙江哈尔滨·期中)已知某固体样品中含有、中的一种或两种。下列说法正确的是
A.取适量样品配成溶液,滴加适量酚酞溶液,若溶液有变红倾向,则样品中只含有
B.取样品在试管中加热,将可能产生的气体通入少量澄清石灰水,若最终仍为澄清溶液,则样品中不含
C.取一定量的样品,利用如图所示装置测定样品中的含量,若球形干燥管增重4.4 g,则所取样品中含有
D.已知固体样品同时含有和,取一定质量的样品配成溶液,滴加溶液至沉淀完全,根据白色沉淀的质量,列方程组,可求出的含量
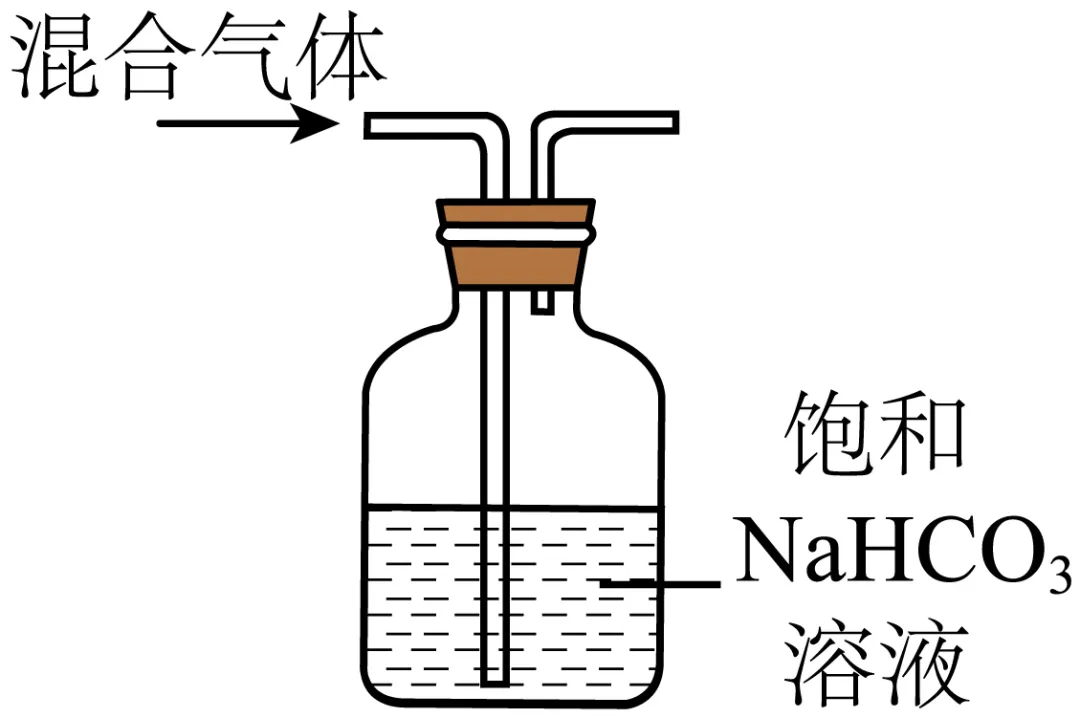
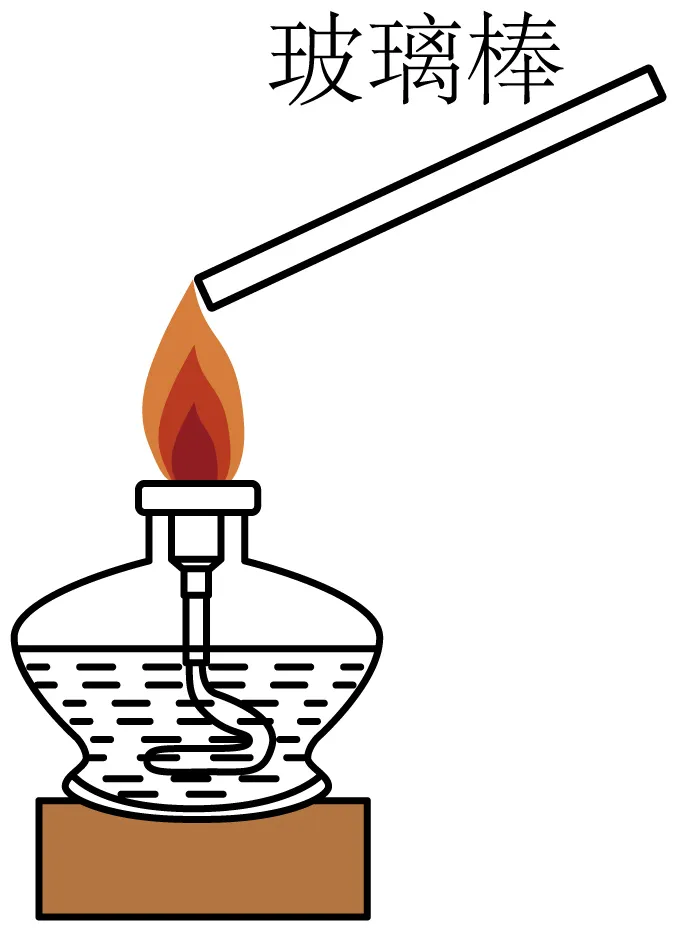
6.(25-26高一上·宁夏银川·期中)利用下列有关实验装置进行的相应实验,能达到实验目的的是
| 
|
A.图Ⅰ除去CO2中含有的少量HCl | B.图Ⅱ检验NaNO3溶液中的钠元素 |
| 
|
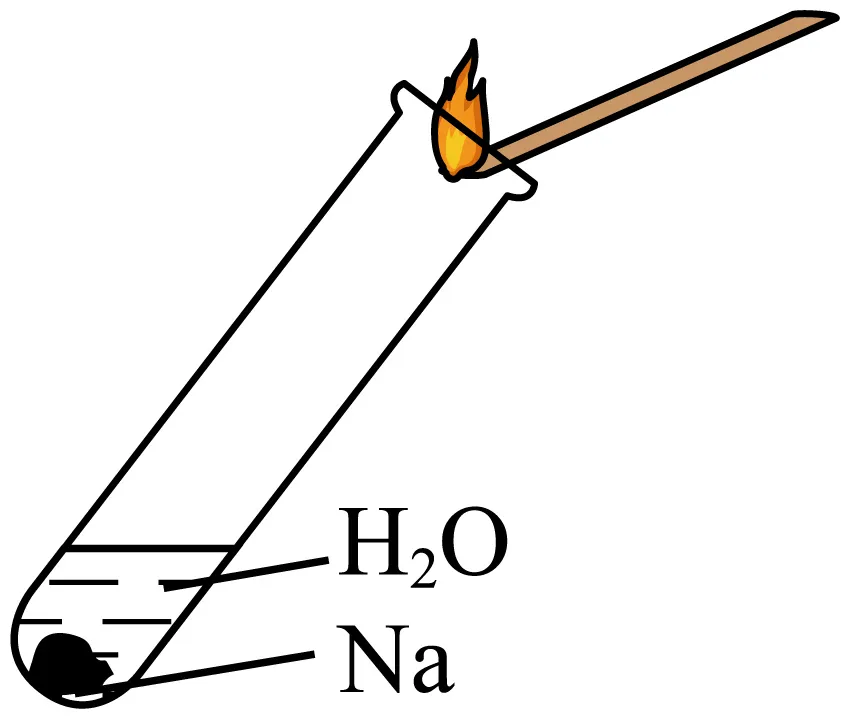
C.检验Na与水反应的气体产物 | D.灼烧金属钠 |
7.(25-26高一上·新疆乌鲁木齐·期中)由我国自主研发的“奋斗者号”潜水艇在太平洋马里亚纳海沟成功坐底,创造了中国载人深潜的新纪录。
(1)过氧化钠可用作潜水艇的供氧剂,写出和反应的化学方程式:,该反应中生成1个分子时,转移个电子。
(2)将一定量的固体投入到含有下列离子的溶液中:,反应完毕后,溶液中上述离子数目几乎不变的有(填离子符号)。
(3)向酸性溶液中加入粉末,观察到溶液褪色,发生如下反应,补全方程式并配平。
_________________________________=_________________________________+___________
(4)某实验小组通过如图所示实验,探究与水的反应,下列说法正确的是___________。
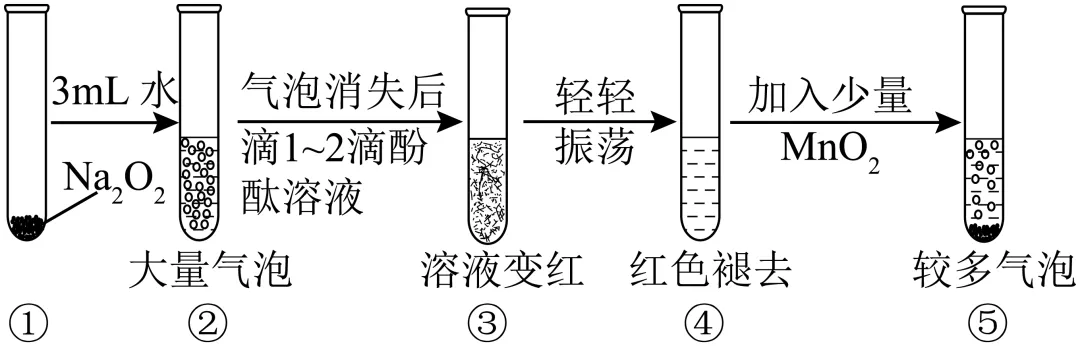
A.②中的大量气泡主要成分是氢气
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是由于溶液中含有强氧化性物质造成的
D.⑤中的主要作用是验证溶液中存在过氧化氢
(5)查阅资料知:在一定条件下可以转化为易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
①已知能发生如下反应:,上述反应中氧化剂是,氧化产物是,HI在反应中体现了性。
②根据上述反应鉴别和NaCl。可选用的物质有(填序号)。
A.水B.碘化钾淀粉试纸C.淀粉D.白酒E.食用白醋bi