【过渡】刚才我们讲了盐酸和硫酸的用途,两者都可用于金属除锈,性质决定用途,说明盐酸和硫酸具有相似的化学性质,下面我们通过实验来探究酸的化学性质。 【问题与预测】(1)结合课题1的内容,预测稀盐酸、稀硫酸能使石蕊溶液和酚酞溶液分别呈现什么颜色。 (2)稀盐酸和稀硫酸是否具有相似的化学性质? 【学生实验】在白色点滴板上分别滴有稀盐酸和稀硫酸,然后再分别滴加紫色的石蕊溶液和无色的酚酞溶液,观察并记录现象。 【实验记录】 | 紫色石蕊溶液 | 无色酚酞溶液 | 稀盐酸 | 变红 | 不变色 | 稀硫酸 | 变红 | 不变色 |
【总结】化学性质1:稀盐酸和稀硫酸都能使紫色的石蕊溶液变为红色,不能使无色的酚酞溶液变色。 【知识回顾】在前面的金属的化学性质学习中,我们知道:在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。根据这一性质,你能写出镁、锌、铁分别与稀盐酸、稀硫酸反应的化学方程式吗? 【学生练习】 Zn+2HCl=ZnCl2+H2↑Zn+H2SO4 =ZnSO4+H2↑ Fe+2HCl=FeCl2+H2↑Fe+H2SO4=FeSO4+H2↑ Mg+2HCl=MgCl2+H2↑Mg+H2SO4=MgSO4+H2↑ 【问题】以上反应的生成物有什么共同之处? 【分析】通常情况下,酸溶液能与活泼金属发生置换反应,生成氢气和该金属的化合物。 【总结】化学性质2:通常情况下,酸溶液能与活泼金属(H之前)发生置换反应,生成氢气和该金属的化合物。 【实验探究】在分别盛有稀盐酸和稀硫酸的试管中各放入生锈的铁钉,过一会儿取出铁钉,用水洗净,铁钉表面和溶液颜色有什么变化? 【实验记录】 | 现象 | 化学方程式 | 铁锈+稀盐酸 | 铁锈溶解,溶液由无色变黄色。 | Fe2O3+6HCl=2FeCl3+3H2O | 铁锈+稀硫酸 | 铁锈溶解,溶液由无色变黄色。 | Fe2O3+3H2SO4=Fe2(SO4)3+3H2O |
盐酸和稀硫酸都能与铁锈(Fe2O3)反应生成黄色的溶液,说明生成了Fe3+。 【问题】以上反应的生成物有什么共同之处? 【总结】化学性质3:酸能与某些金属氧化物反应生成水和该金属的化合物。注意:反应前后化合价不变! 【问题】利用上面的反应可以清除铁制品表面的锈,除锈时能否将铁制品长时间浸在酸中?为什么? 【讲解】反应初期,是酸溶液与铁锈发生了反应;铁锈消失后,酸溶液又与铁发生了反应。即: Fe2O3+6HCl=2FeCl3+3H2OFe2O3+3H2SO4=Fe2(SO4)3+3H2O Fe+2HCl=FeCl2+H2↑Fe+H2SO4=FeSO4+H2↑ 所以不能将铁钉长时间浸泡在酸溶液中,因为酸会继续与铁发生反应,造成铁被腐蚀。 【结论】根据以上实验与分析,结合前面学过的知识,归纳稀盐酸、稀硫酸等酸有哪些相似的化学性质。 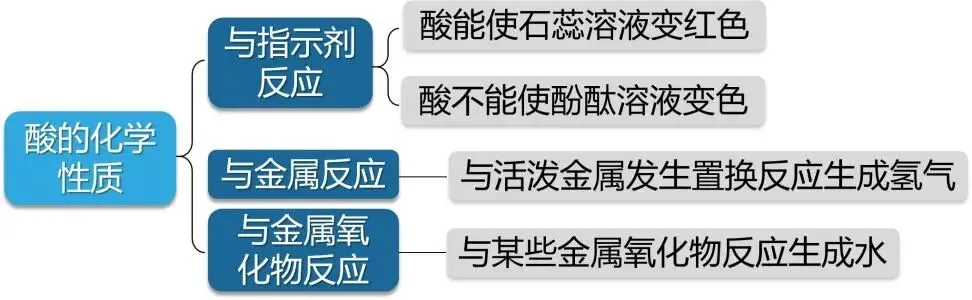
【思考】稀盐酸、稀硫酸等酸为什么会有相似的化学性质呢? 【实验10-7】分别试验稀盐酸、稀硫酸、蒸馏水和乙醇的导电性(可以将小灯泡换成发光一极管)。 【学生活动】观看实验视频,观察并记录现象,思考原因。 【实验记录】 | 盐酸 | 硫酸 | 蒸馏水 | 乙醇 | 灯泡 | 亮 | 亮 | 不亮 | 不亮 | 导电性 | 导电 | 导电 | 不导电 | 不导电 |
【交流讨论】稀盐酸、稀硫酸溶液都导电,而蒸馏水、乙醇不导电,这说明了什么? 【总结】1.溶液导电说明了溶液中存在着自由移动的带电粒子。 2.盐酸、硫酸这样的酸在水溶液中都能解离出H+和酸根离子,所以酸在溶液中解离的阳离子全是H+,这就是酸具有相似的化学性质的原因。 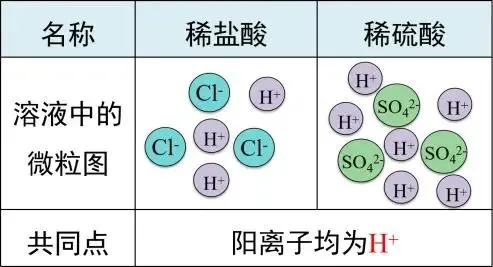
【对应训练3】草酸是自然界中普遍存在的一种酸,推测它不可能具有的化学性质或用途是 ( ) A. 能用于除铁锈 B. 能与二氧化碳反应 C. 能与酸碱指示剂作用 D. 能用于除水壶内的水垢(CaCO3) 【答案】B 【对应训练4】用足量的盐酸浸泡生锈的铁钉,可观察到的实验现象是() ①铁钉上的铁锈消失; ②铁钉上有气泡产生; ③溶液呈黄色。 A.只有①②B.只有①③ C.只有③D. ①②③ 【答案】D 【对应训练5】不同的酸具有相似化学性质的原因是() A.它们都含有酸根 B.它们都含有氢元素 C.它们溶于水后都能解离出H+ D.它们都含有氧元素 【答案】C 【对应训练6】如图是稀硫酸与不同物质之间发生化学反应的颜色变化 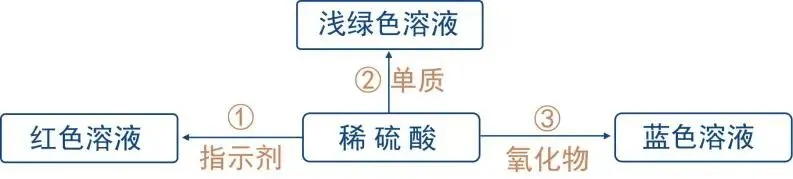
(1)①处所使用的指示剂是; (2)请你在编号②③处各填入一种物质。②是;③是; (3)反应②涉及的基本反应类型是; (4)如果想要得到黄色溶液,那么有稀硫酸参与反应的方程式。 【答案】紫色石蕊溶液,铁,氧化铜,置换反应,Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O |